Introducción:
El síndrome respiratorio bovino (SRB) se define como el proceso neumónico o bronconeumónico provocado por diferentes agentes biológicos y factores predisponentes, del animal y del sistema de producción intensivo, característico del bovino y que adquiere especial importancia y gravedad cuando se trata de animales jóvenes.
El SRB está considerado como la patología con mayor repercusión en la industria del bovino de carne, y está presente en los distintos sistemas y etapas de producción, aunque en este artículo nos centraremos en el ternero de cebo. A pesar de que en los últimos años se han realizado avances en el conocimiento de los agentes patógenos y los factores de riesgo asociados, debemos reconocer que la incidencia de SRB no ha disminuido manteniéndose en niveles similares en los últimos veinte años. En ganado de cebo las cifras de incidencia son variables entre el 30-50% de morbilidad, pudiendo llegar en algunos casos al 80%.
La complejidad del SRB es que a pesar de ser un proceso infeccioso su control pasa por tener en cuenta la etiopatogenia multifactorial y de manejo. A lo largo de este artículo revisaremos todos los factores que intervienen en el desarrollo de este síndrome, así como las estrategias de prevención y control que existen para minimizar su incidencia así como la gravedad de sus consecuencias a nivel sanitario y productivo.
Consecuencias productivas e impacto económico:
El SRB representa el 70% de la patología del cebadero. La presencia de este síndrome repercute directamente en el crecimiento de los animales, con datos de reducción del 7,2% de peso vivo o 0,5-0,8 kg menos de ganancia media diaria.
A nivel económico, podemos asegurar que es la patología con mayor impacto en el ternero de cebo. Las pérdidas son difíciles de cuantificar ya que debemos contemplar costes indirectos, como la disminución de productividad del animal, y costes directos derivados de la prevención, tratamientos, incremento de mano de obra, asistencia veterinaria, animales crónicos y mortalidad. El cálculo de costes varía según el tipo de explotación y las condiciones de manejo, lo cual hace que existan diferentes datos en los estudios a nivel mundial.
En Estados Unidos un estudio de 5.976 terneros analizó la influencia de varios factores en el valor comercial del ganado. Mostró datos de incidencia de SRB de 8,17% siendo la causa de muerte del 49% de las bajas. Además según este estudio, el ganado que sufre SRB tiene una pérdida de valor respecto al animal sano que va desde 23,23 a 151,18 $; una vez contabilizados los costes veterinarios, el menor rendimiento, el menor valor de las canales, las pérdidas por mortalidad y sacrificio antes de la finalización (Smith, 2009).
En 2011 el Departamento de Agricultura de Estados Unidos (USAD) publicó que el 16,2% del ganado de engorde desarrolló SRB, con un coste medio de tratamiento 23,60 $, aún con datos de mortalidad asociada a SRB de tan sólo 1,42 %.
En España, un estudio económico estimó el impacto económico promedio por cabeza del SRB en 61,36 €/animal (Yus, 2007), lo cual incluía:
- reducción GMD: 14,15 €, considerando impacto de enfermedad clínica y subclínica.
- mortalidad: 12,99 €; con un 3,1% de mortalidad, considerando animales de 4 meses de edad (compra, consumo, gastos fijos, intereses).
- pérdidas por sacrificio prematuro: 14,39 €; 4% de sacrificios prematuros a una edad de 6 meses.
- gastos de veterinario y tratamientos: 7,57 €, considerando 2,1 tratamientos/animal y 10 terneros tratados por consulta (coste del tratamiento y servicio veterinario).
- programas preventivos: 12,16 €.
Figura 1: impacto económico promedio por ternero
Etiología multifactorial:
El primer factor predisponente para el desarrollo de patología respiratoria es el propio animal. En el caso del bovino nos encontramos un árbol traqueobronquial largo y unos pulmones pequeños en relación a su tamaño corporal. Estas características anatómicas hacen que sea más sencillo el que se depositen partículas a lo largo de las vías respiratorias, siendo su expulsión más costosa por la longitud de estas.
Otra particularidad es la existencia del bronquio traqueal propio del pulmón derecho. A menudo las bacterias y partículas que deberían ser eliminadas gracias a la barrera mucociliar y procesos de expulsión, retornan y se introducen en el bronquio traqueal. Esto da lugar al desarrollo de neumonía, siendo siempre el lóbulo craneal derecho el primero y más afectado en el SRB.
Debido a la presencia de septos interlobulares decimos que el pulmón bovino es un pulmón muy compartimentado. Este tejido conectivo rodea cada segmento broncopulmonar de forma independiente, lo cual limita la ventilación colateral y el movimiento de aire entre las distintas partes del pulmón. A esto hay que sumarle que los alveolos bovinos tienen un bajo número poros de Kohn, es decir, poca capacidad de intercambio gaseoso entre ellos. Este problema de comunicación y compensación entre las distintas partes del pulmón en presencia de una infección va a dar lugar a alteraciones compensatorias, con lesiones como el enfisema.
Por último, existen diferentes mecanismos inmunitarios que buscan mantener la esterilidad dentro del pulmón bovino. En vías altas, nariz y faringe encontramos una microbiota compuesta por bacterias de diversos géneros (Bacillus, Streptococcus, Streptomyces, Micrococcus, Pseudomonas) compitiendo con gérmenes patógenos; mientras que las vías bajas deberían ser estériles. El sistema mucociliar evita que estos microorganismos y otras partículas extrañas lleguen a vías bajas, pero el correcto funcionamiento de este puede verse ralentizado por agentes irritantes, enfermedades crónicas, infecciones víricas, deshidratación y taquipnea.
En las secreciones del aparato respiratorio encontramos diferentes moléculas con capacidad de opsonización que facilitan la fagocitosis eliminando los posibles gérmenes presentes. Además, el tejido linfoide asociado a mucosas (MALT), los linfocitos T y Natural Killer participan en la defensa frente a virus y bacterias.
Esta respuesta inmune, innata y adaptativa, va a verse alterada por el estrés y el consecuente aumento de cortisol en los animales, o por infecciones primarias víricas.
Dentro de la etiología multifactorial, el ambiente y el estrés que produce sobre el ternero son unos de los factores más importantes en la presentación del SRB.
Edad: al tratarse de animales jóvenes nos encontramos con un pulmón inmaduro y con poca exposición a agentes patógenos. En España, estos animales son trasladados desde las explotaciones de vacas nodrizas en extensivo tras el destete (ternero pastero) o desde las explotaciones lecheras a las pocas semanas de vida (ternero mamón), a las explotaciones de cebo. Esta transición y los manejos posteriores producen estrés y, por tanto, peor respuesta inmunitaria a patógenos, en comparación con ganado adulto.
Origen y transporte: debido al gran tamaño de los cebaderos respecto a las explotaciones de origen nos encontramos con multitud de orígenes en los animales que componen cada lote. Esto es conocido como “efecto guardería”: se produce una exposición de animales jóvenes inmunológicamente inmaduros a agentes patógenos de diferentes grados de virulencia. Unido al estrés del transporte, la manipulación de animales y el agrupamiento, suponen un punto clave en el desencadenamiento del SRB.
Densidades altas: el establecimiento de jerarquías tras hacer los lotes es otra causa de estrés en los animales. Los animales dominantes van a ejercer presión sobre los más débiles a la hora de comer, beber o descansar, por lo que es muy importante evitar el hacinamiento. La heterogeneidad de lotes en edades y pesos va a agravar este estrés jerárquico, por lo que es algo que debe evitarse, así como la introducción de animales nuevos en un lote ya establecido. Las recomendaciones son de 5 m2/ animal, en ternero pastero, o 1m2/ 100 kg de peso vivo, y parques o corrales de no más de 30 animales.
Figura 2: corral con hacinamiento
Instalaciones: es primordial facilitar el acceso al agua y comida, así como corrales confortables y secos para que los animales puedan descansar. La correcta hidratación y nutrición de los animales es básica para el funcionamiento del sistema inmune del ternero frente los patógenos del SRB. Un mal diseño de las instalaciones va a dar lugar a corrientes de aire, o por el contrario, poca ventilación con altos niveles de humedad, calor y gases ambientales que facilitan el contagio de estos patógenos.
Figura 3: bebedero con agua limpia y de fácil limpieza
Los agentes patógenos implicados en el SRB están presentes en la mayoría de las explotaciones bovinas, y es bajo condiciones de estrés cuando van a dar lugar a patología. Normalmente los virus, por su papel inmunodepresor y su acción sobre el sistema mucociliar, van a ser la vía de entrada de la enfermedad. Tras esta primera infección vírica son las bacterias, habitantes habituales de nasofaringe, las que de forma oportunista van a ser capaces de proliferar y colonizar el pulmón produciendo lesiones y mortalidad.
- Víricos:
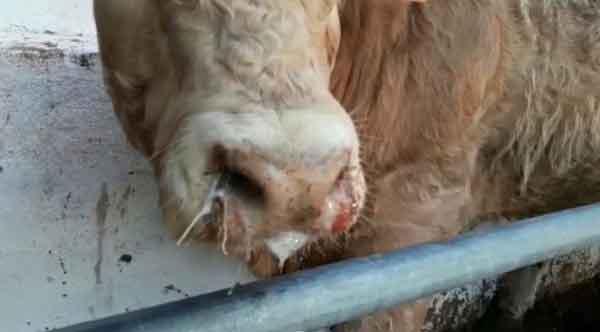
- Herpesvirus Bovino tipo 1 (BHV-1): este herpesvirus en animales jóvenes va a dar lugar a rinotraqueítis infecciosa bovina (IBR), por infección de las vías respiratorias altas, conjuntivitis e inmunosupresión. Tiene un papel importante en el SRB ya que inhibe la respuesta inmune y ataca la mucosa del árbol bronquial, lo que facilita la posterior colonización bacteriana. Típicamente produce lesiones ulcerativas blanquecinas en mucosas oculares y nasales, que evolucionan a rinitis mucopurulentas y traqueítis fibrinosa en casos graves.
Figuras 4 y 5: traqueítis y traqueítis fibrinosa típicas de BHV-1
Tras la infección primaria se produce latencia del virus a nivel de ganglio trigémino, por lo que el animal se convierte en portador de por vida, y en momentos de inmunosupresión va a excretar de nuevo el virus contagiando a nuevos animales. Además, la existencia de planes de control y erradicación de este virus en Europa, y recientemente también a nivel nacional en España, hace que existan animales procedentes de zonas con baja prevalencia y sin ningún tipo de exposición previa al virus, que tras el transporte y el agrupamiento con otros animales presentan brotes graves de enfermedad.
Figura 6: ternero pastero con signos de rinotraqueítis infecciosa bovina
- Virus Respiratorio Sincitial Bovino (BRSV): es el virus más frecuentemente implicado en el SRB, sobretodo en animales recién destetados o sometidos a estrés. Produce necrosis de las células epiteliales bronquiales con formación de sincitias e inhibición de macrófagos alveolares, lo que da lugar a neumonía broncointersticial principalmente en áreas craneoventrales del pulmón. La evolución de estas lesiones es agravada por la respuesta exagerada del sistema inmune del favoreciendo una mayor adherencia de bacterias. En cuadros graves alcanza altos niveles de morbilidad y mortalidad.
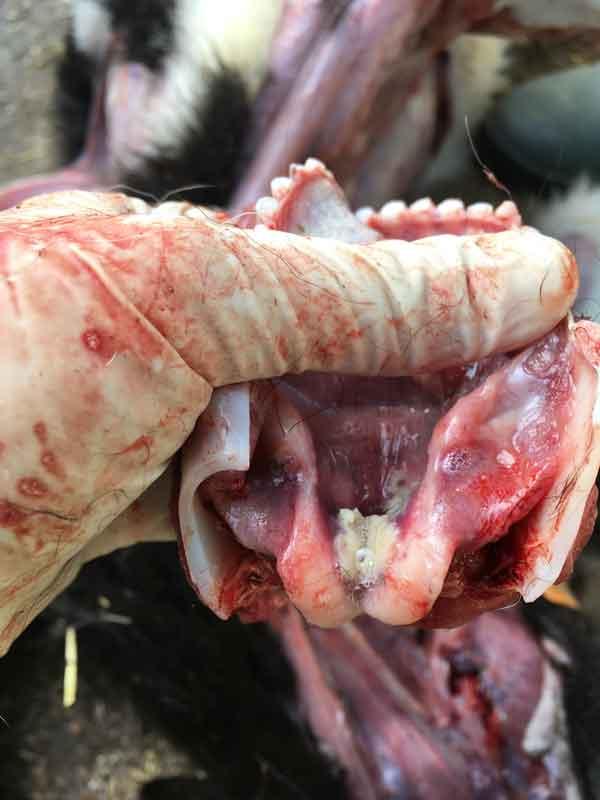
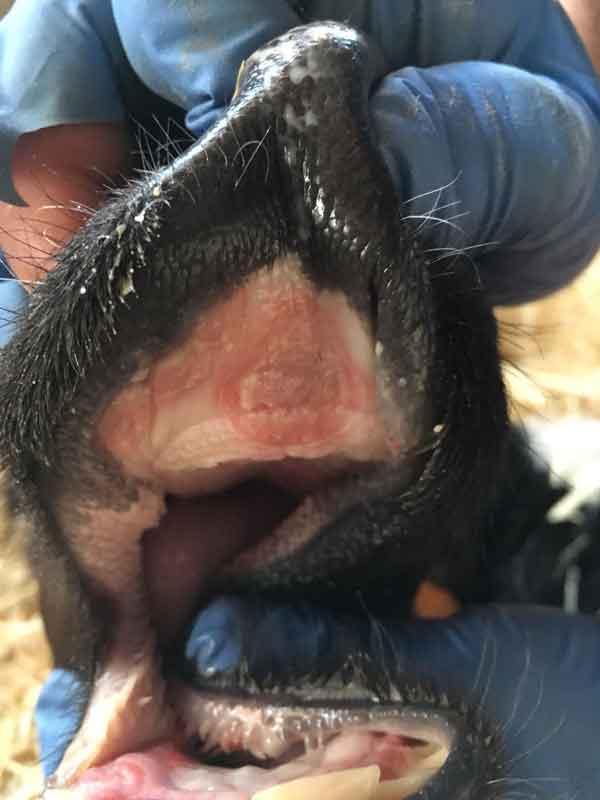
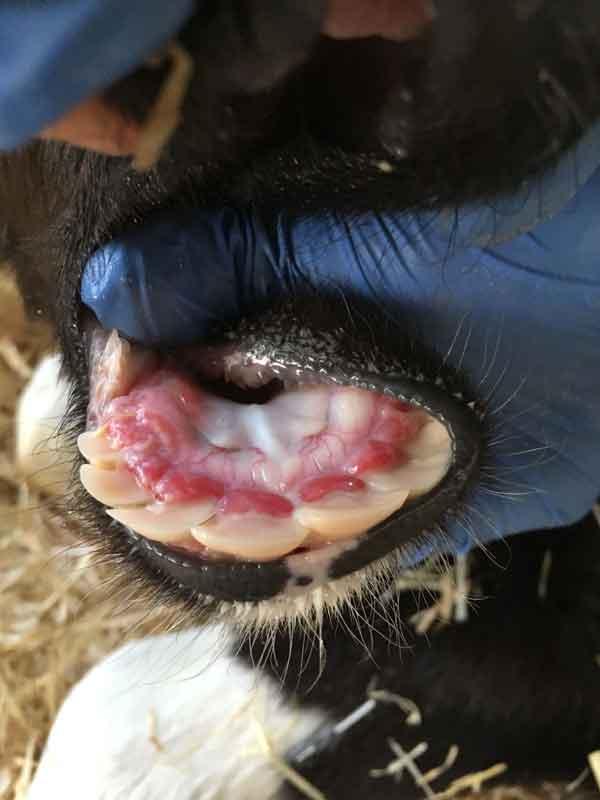
- Virus de la Diarrea Vírica Bovina (BVD): su principal acción es inmunodepresora a nivel general en el animal, pero además es capaz de infectar de forma primaria los macrófagos alveolares facilitando la infección bacteriana posterior. Está muy presente en los cebaderos de forma subclínica (70-90% de prevalencia) por lo que es un patógeno que no debemos subestimar.
Figuras 7 y 8: lesiones en mucosa oral típicas de BVD
- Parainfluenza tipo 3 (PI-3): este virus muy presente en la población bovina es sólo grave en animales jóvenes, adultos bajo condiciones estresantes, o en sinergia con otros patógenos. Tiene acción sobre vías altas y bajas afectando al aparato mucociliar e inhibiendo los macrófagos alveolares, pero con menor gravedad que el BRSV.
- Bacterianos:
- Mannheimia haemolytica: durante años ha sido la principal bacteria aislada en casos mortales de SRB. Cuando la carga infecciosa es alta puede ser patógeno primario sin la necesidad de infección vírica o estrés previo. Debido a sus factores de virulencia, principalmente la leucotoxina o exotoxina LKT, es responsable de casos agudos y con alta mortalidad de SRB. Esta toxina es producida en altas cantidades destruyendo macrófagos y neutrófilos en pulmón y necrosis del parénquima pulmonar por acción de enzimas proteolíticas. Como lesiones características de la manhemiosis veremos bronconeumonía fibrinosa y pleuritis fibrinosa.
Figura 9: necrosis, hemorragias y septos distendidos típicos de neumonía por M. haemolytica
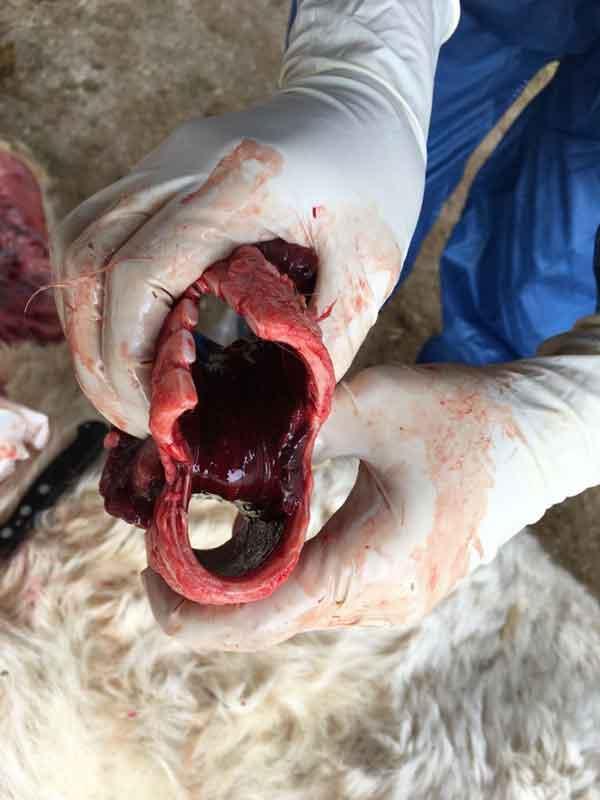
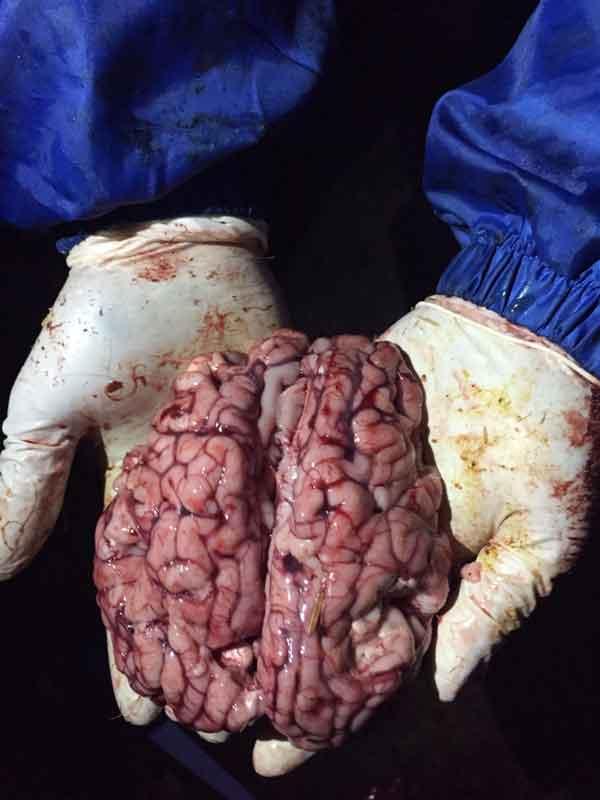
- Histophilus somni: hasta hace unos años era una bacteria poco diagnosticada en nuestro país, al contrario que en países como Canadá y Estados Unidos. Con la mejora de las técnicas de diagnóstico, principalmente técnicas moleculares como la PCR, ha aumentado su diagnóstico. En España existen datos de un 49% de positividad en muestras de pulmón cuya causa de muerte fue SRB (DIAGNOS HIPRA, 2006). Su principal factor de virulencia es una endotoxina de tipo lipooligosacarido (LOS), que produce vasculitis y trombosis a nivel capilar. Da lugar a enfermedad pulmonar con bronconeumonía y pleuritis fibrinosa (histofilosis). Pero además, tras una diseminación hemática, puede producir miocarditis, pericarditis fibrinosa, peritonitis, septicemia, artritis y meningoencefalitis tromboembólica (TEME o enfermedad del sueño).
Figura 9: meningoencefalitis tromboembólica
- Pasteurella multocida: aunque está presente en los aislamientos de SRB se considera menos importante ya la bacteria tiene menos factores virulencia que contribuyan a su patogenicidad primaria. Produce una endotoxina de lipopolisacáridos que puede dar lugar a bronconeumonía supurativa lobulillar con cuadros clínicos más largos y menos agresivos.
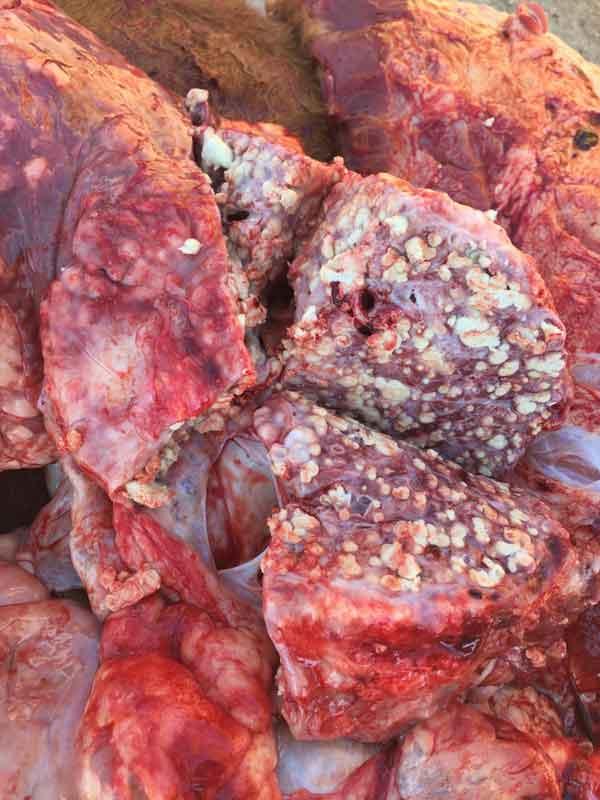
- Mycoplasma bovis: a pesar de no ser un agente primario y estar casi siempre asociado a infecciones crónicas producidas por las bacterias citadas anteriormente, este agente tiene especial importancia en el SRB por las pérdidas que produce a largo plazo en las explotaciones: animales crónicos, uso repetido de antibióticos y mortalidad. Produce neumonía con nódulos caseonecróticos, y en casos avanzados puede producir otitis media y artritis. Actualmente no existen vacunas disponibles en el mercado para su prevención, y su control con antibióticos supone en la mayoría de los casos un fracaso. Carece de pared celular por lo que los β-lactámicos no van a ser eficaces y tampoco las sulfamidas por no poseer ácido fólico.
Figura 11: nódulos caseonecróticos típicos de M. bovis
Prevención y tratamiento:
La transferencia de inmunidad materna reduce el riesgo de padecer SRB, por lo que el primer punto clave en la prevención sería asegurar la ingesta de calostro de calidad. Además, se ha demostrado un aumento de inmunidad específica en terneros cuyas madres fueron vacunadas frente a gérmenes productores de SRB.
Como hemos visto la entrada al cebadero, y el destete cuando se trata de terneros mamones, son momentos críticos para el desarrollo de la enfermedad. Es en este punto cuando necesitamos mayores niveles de inmunidad específica en los animales, para ello lo ideal sería realizar un acondicionamiento previo o “preconditioning” en las explotaciones de origen. Este acondicionamiento, muy extendido en países como Estados Unidos, consiste en desparasitar, vacunar y adaptar al pienso a los animales previamente al transporte y la llegada al cebadero. Este sistema ha demostrado ser exitoso aunque pueda resultar utópico tal y como se desarrolla la comercialización de los terneros desde las explotaciones de origen en nuestro país.
Hoy en día, la gran mayoría de los terneros llegan al cebadero sin este protocolo previo por lo que debemos implantar un protocolo de vacunación a la llegada. Se recomienda esperar unas 12-24h tras la descarga, de manera que el animal pueda beber, comer, descansar, identificar el nuevo entorno y disminuir así sus niveles de estrés antes de cualquier manejo.
El protocolo de vacunación debe estar adaptado al cebadero y a los patógenos existentes en él, aunque como hemos visto los patógenos responsables son ubicuos por lo que lo más sensato es realizar protocolos vacunales completos.
Lo más habitual es utilizar vacunas multivalentes víricas vía parenteral, aunque el uso de vacunas vía intranasal es más que interesante en animales jóvenes por dos motivos principales: con la vía intranasal conseguimos evitar los fallos vacunales por interferencia con anticuerpos maternales, que además no son completamente protectivos al no estar presente localmente, y para favorecer el aumento de la inmunidad específica a nivel local y respuesta de IgA en tracto respiratorio superior.
En el caso del BRSV las vacunas vivas han demostrado ser más eficaces y rápidas en la protección que las inactivadas (Sacco, 2014). Otro punto a tener en cuenta en el plan vacunal es el uso de vacunas vivas marcadas de BHV-1, dados los avances en los planes de control de IBR y los requisitos sanitarios de exportación de los animales. Se tratan de vacunas vivas modificadas, deleccionadas en la glicoproteína E (-gE) para el marcaje serológico y la atenuación. Una de estas vacunas incluye también la delección de la timidinkinasa (-tK), enzima responsable del neurotropismo y acantonamiento de este virus, con ello se mejora la atenuación del virus vacunal asegurando la estabilidad y seguridad de este. Este tipo de vacunas están siendo cada vez más utilizadas y han demostrado ser muy eficaces en la prevención y el control de la rinotraqueítis infecciosa bovina (Thiry, 2006).
Respecto a las vacunas bacterianas, encontramos en el mercado vacunas frente a M. haemolytica como bacterinas inactivadas o suspensiones con leucotoxoides, siendo éstas últimas las que han demostrado tener mayor eficacia en la prevención de síntomas clínicos y daño pulmonar (Rice, 2007). Además, ya existe en Europa una vacuna que incluye protección frente a Histophilus somni, bacteria como hemos visto muy prevalente y con graves consecuencias ya que no sólo produce problemas neumónicos.
El uso de antibióticos de larga duración, principalmente macrólidos, aplicados en masa a la entrada de los animales en el cebadero o antes de un manejo estresante ha sido utilizado durante años como estrategia de prevención frente al SRB. A día de hoy, y dentro del marco de la reducción del uso de antibióticos, es una práctica a evitar.
Siendo el estrés sufrido por los animales una de las principales causas del desencadenamiento del SRB es un punto donde debemos poner el foco a la hora de mejorar. En bovinos está considerado como estrés crónico cuando un animal está sometido a este más de 48h, y sabemos que esto produce inmunosupresión durante al menos una semana. La calidad del encamado, evitar la sobrepoblación, el aislamiento de las malas condiciones meteorológicas, pero garantizando buena ventilación, el acceso a agua limpia y comida apetecible y de calidad que garantice un buen estado de hidratación y nutricional, son aspectos básicos que han demostrado aumentar la resistencia de los terneros a la enfermedad.
Una vez establecido el proceso patológico es fundamental instaurar un tratamiento adecuado que controle la enfermedad y minimice sus consecuencias. Este debe contemplar soporte, uso de antimicrobianos, antiinflamatorios, y en algunos casos vacunación de urgencia.
El soporte debe basarse en asegurar la hidratación de los animales, fundamental para la calidad del moco, el funcionamiento de las cilias y disminuir el posible estrés metabólico.
En cuanto al tratamiento antibiótico debemos usar moléculas con indicación terapéutica para el SRB, respetando la dosificación y la duración del tratamiento. Dado que los procesos infecciosos en bovino tienden a cronificar un tratamiento mínimo debe ser de 3 a 5 días, manteniendo niveles terapéuticos en sangre al menos 7 días, pudiendo alargarlo si no se ha conseguido una recuperación completa. Cambiar de antibiótico demasiado pronto induce a la aparición de resistencias por lo que debemos esperar mínimo al tercer día de tratamiento para decidir si continuar el tratamiento o cambiarlo. El registro de tratamientos en el cebadero es fundamental para valorar el fracaso o éxito de estos. Una tasa de curación del 80% tras el primer tratamiento se considera buena, teniendo que tratar un 20% de los animales una segunda vez. Tras tres tratamientos sin curación debemos considerar el animal como crónico y la recomendación es separarlo del resto de los animales.
El uso de antiinflamatorios está aconsejado ya que disminuye la reacción inflamatoria responsable de las lesiones pulmonares, la fiebre y el dolor. En este punto debemos ser cuidadosos y tener en cuenta que el uso prolongado de AINEs puede dar lugar a la aparición de úlceras gastrointesionales, y que el uso de corticoesteroides es inmunosupresor, lo cual es contraproducente en algunos casos.
Diagnóstico precoz:
Otra de las dificultades del SRB es que cuando el animal muestra los primeros signos evidentes de enfermedad nos encontramos con lesiones pulmonares avanzadas, es decir, llegamos tarde y esto reduce enormemente el éxito del tratamiento. Es por ello que debemos trabajar en el diagnóstico precoz de la enfermedad.
- Observación de los animales y toma de temperatura:
Entrenar al personal del cebadero para evaluar a los animales es clave en el diagnóstico temprano. Se recomienda realizar un examen de los animales un mínimo de dos veces al día. Para ello una vez dentro del corral debemos mover despacio los animales, observando que tienen un comportamiento normal y que no existen signos de depresión (animales letárgicos que a veces se aíslan). Una buena forma de trabajar es fijarse dentro del corral en puntos clave como:
- Aspecto del pelo y condición corporal
- Grado de llenado del rumen en el ijar izquierdo
- Presencia de diarrea o estreñimiento
- Descarga ocular
- Descarga nasal
- Posición de las orejas
- Tos o dificultad respiratoria
Si encontramos anormalidad en uno o varios de estos puntos el animal es sospechoso de enfermedad y debemos sacarlo del corral para explorarlo de forma individual y tomar temperatura rectal. Una vez realizada la exploración individual un buen punto de corte para el diagnóstico de SRB es la presencia de temperatura rectal superior a 39,7º C y presencia de alteraciones a nivel respiratorio como descarga ocular, descarga nasal, orejas caídas y tos. Existen diversos sistemas que nos ayudan a valorar todos estos signos y asignar una puntuación o “score” para el diagnóstico de SRB. Uno de los más utilizados es Calf Health Scorer (School of Veterinary Medicine University of Wisconsin-Madison), que a pesar de estar diseñado para valorar la enfermedad en novillas de recría de leche podemos adaptar al cebadero con facilidad.
En los últimos años se han realizado avances en cuanto al protocolo y los criterios del examen ecográfico de la cavidad torácica, sobretodo en terneros lactantes por la facilidad de manejo, como herramienta para diagnosticar precozmente la enfermedad. Es necesario una sonda lineal con profundidad baja (7,5 MHz) para diagnosticar consolidaciones pulmonares. En animales jóvenes de entre 60 y 80 días podemos usar alcohol y en animales de más tamaño será necesario el afeitado de los espacios intercostales y el uso de gel ecográfico. Debemos explorar los espacios intercostales (costillas 4 a 11) de caudal a craneal y de ambos lados siempre, siendo metódicos y consistentes. Aunque su uso a nivel de explotación todavía no está extendido, es una técnica económica y que con entrenamiento, un buen protocolo de exploración y de recogida de datos puede ser de gran utilidad en la detección precoz de animales enfermos.
Figura 12: realización de ecografía torácica en ternero lactante
- Toma de muestras y diagnóstico laboratorial:
El diagnóstico etiológico de los patógenos presentes en el SRB es interesante desde el punto de vista de explotación y nos permite tomar decisiones respecto al programa de vacunación, la selección del antibiótico, mejoras en bioseguridad y de corrección de la causa, pero no tanto a nivel individual ya que es costoso y normalmente no obtenemos los resultados de forma inmediata.
La serología nos va a dar una idea de los patógenos a los que han estado expuestos los animales, y en caso de que podamos ver seroconversión en dos serologías separadas podremos confirmar un contacto con el virus, aunque no que éste sea responsable del proceso.
Los cultivos de muestras de hisopos nasofaríngeos profundos se utilizan con frecuencia por la facilidad de recogida en condiciones de campo, aunque el aislamiento de un patógeno en este punto no tiene por qué estar dando lugar a enfermedad. Con lavados bronquioalveolares o transtraqueales obtenemos una muestra de una parte más baja del tracto respiratorio del animal pero de nuevo no está claro que el ailsamiento de un patógeno sea indicativo de enfermedad por ese microorganismo. Lo ideal sería tomar una muestra del pulmón in vivo, para ello se han realizado a nivel experimental biopsias pulmonares mediante toracoscopia obteniendo buenos resultados.
En cuanto al método laboratorial a utilizar, el cultivo microbiológico es económico y nos puede dar información sobre la sensibilidad a antibióticos, pero puede ser un diagnóstico lento y poco preciso ya que la sensibilidad se ve afectada por infecciones concomitantes y los tratamientos antibióticos. Sin embargo hoy en día el avance y el abaratamiento en el coste de las técnicas moleculares como la PCR supone una ventaja en cuanto a rapidez y sensibilidad del diagnóstico de estos patógenos existiendo tanto PCR simples como múltiples que combinan distintos patógenos del SRB.
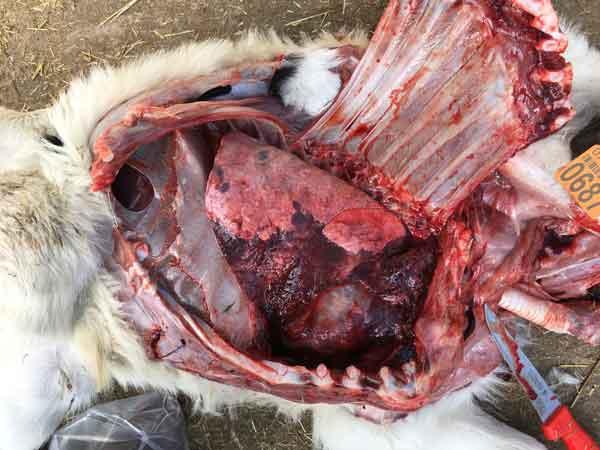
El diagnóstico postmortem debería realizarse como protocolo en todos los animales que son baja en la explotación. Es un diagnóstico de campo que resulta económico, rápido y que va a aportarnos mucha información sobre los distintos procesos patológicos del cebadero. Nos permite tomar muestras para las distintas técnicas diagnósticas y realizar un diagnóstico presuntivo mediante las lesiones que identifiquemos. Se debe realizar de forma protocolizada y completa, y no centrarnos sólo en el aparato respiratorio. La toma de muestras deberá hacerse siempre lo antes posible y en condiciones de higiene que eviten posible contaminaciones, y estas deberán conservarse para su envío siguiendo las indicaciones del laboratorio.
Un buen registro de las necropsias realizadas, los hallazgos patológicos encontrados y los resultados de laboratorio nos ayudará a tomar correctamente decisiones profilácticas y de tratamientos a nivel de explotación.
Figura 13: necropsia en ternero lactante.
Conclusiones:
Una vez revisado el SRB, su etiología multifactorial y sus graves repercusiones a nivel sanitario y económico, es importante que como veterinarios trabajemos para minimizar las consecuencias de este. Debemos poner el foco en la prevención, con el uso de vacunas que aumenten inmunidad específica frente a los diferentes patógenos, mejoras en el manejo que reduzcan el estrés de los animales, e implementando protocolos de diagnóstico precoz y específico que nos permitan detectar la enfermedad lo antes posible.
Artículo publicado originalmente en Revista Badajoz Veterinaria