Manejo del comedero y del bebedero en la dosificación de antibióticos en Porcinos
Publicado: 4 de febrero de 2013
Por: Jérôme del Castillo, D.M.V., M.Sc., Ph.D.Université de Montréal, Canadá
INTRODUCCIÓN
El control de las enfermedades infecciosas es de suma importancia en producción porcina, debido especialmente al agrupamiento de los animales en locales con alta densidad poblacional. Por una parte, esta situación favorece la proliferación de agentes patógenos y su trasmisión entre los animales. Además, ciertos eventos inevitables en el manejo de la piara (por ejemplo, el destete de los lechones y su transporte a las naves de recría) son causas de estrés que disminuye la resistencia natural de éstos contra los agentes patógenos. Por tanto, la estrategia de control de las infecciones debe de actuar tanto sobre éstos como sobre los factores de riesgo presentes en la piara.
Los antibióticos empleados en terapias poblacionales se administran con mayor frecuencia por vía oral. Dado el carácter insumiso de los cerdos, el alimento y el agua que éstos consumen de manera espontánea son unos vehículos muy ventajosos para la dosificación de fármacos, porque ambos alcanzan a tratar un número ilimitado de cerdos, sin estresarlos ni sobrecargar de trabajo a los porcicultores. Pero la eficacia terapéutica del pienso o del agua fortificada con antibióticos depende no solo de la sensibilidad del agente patógeno al antibiótico, sino también de la manera en que los animales toman voluntariamente su tratamiento. Si ésta es inadecuada con respecto a las propiedades farmacocinéticas y farmacodinámicas de la droga, se incrementará el riesgo de fracaso terapéutico, de demora en la resolución de la infección o de recaer tras cesar el tratamiento. Este artículo examina los principales factores que determinan la eficacia de los antibióticos y discute de los factores relativos al manejo del comedero y del bebedero que permiten mejorar su uso terapéutico poblacional cuando son administrados por vía oral.
EFICACIA TERAPÉUTICA Y EXPOSICIÓN SISTÉMICA AL ANTIBIÓTICO
La mortalidad microbiana causada por los antibióticos puede resultar de la activación directa de los mecanismos de autodestrucción del microorganismo (fluoroquinolonas, aminoglucósidos y penicilinas) o bien resultar indirectamente de la disminución del metabolismo de éste, lo que agota sus reservas proteicas, energéticas o de nucleótidos (tetraciclinas, macrólidos, pleuromutilinas, lincosamidas, fenicoles y sulfamidas). La acción terapéutica del antibiótico no solo se limita a la mortalidad del agente infeccioso: los inhibidores del metabolismo también disminuyen la expresión de sus factores de virulencia (toxinas, adhesinas, feromonas, etc.) y ciertos moderan la intensidad de la reacción inflamatoria en el foco infeccioso (tetraciclinas).
La farmacodinamia del antibiótico (esto es, la magnitud su efecto) siempre es proporcional al porcentaje de receptores que éste ocupa en el agente infeccioso. In vivo, este porcentaje de ocupación depende de la cantidad de antibiótico presente en el foco infeccioso, que difícilmente se puede medir con fiabilidad y de manera inocua en el animal. Sin embargo, ésta se puede estimar promedio de los estudios farmacocinéticos: la concentración plasmática (Cp) del antibiótico es un marcador de su exposición sistémica (esto es, la cantidad presente en el medio interno del animal).La Cp de una muestra indicará el nivel de exposición instantáneo al antibiótico, mientras que el área bajo la curva (ABC) de la Cp en función del tiempo indicará la exposición acumulada que se obtiene con la dosis administrada. Dado que la circulación sanguínea es el vehículo de difusión del fármaco en el organismo, la Cp también estimará la exposición al antibiótico en el foco infeccioso.
La farmacocinética es el estudio del tránsito del fármaco a través del organismo, desde el instante de dosificación hasta el de su completa eliminación. Este tránsito se descompone en una serie de procesos (Liberación, Absorción, Distribución y eliminación por Metabolismo y/o Excreción) que ocurren simultáneamente y cuyas importancias relativas varían en función del tiempo. El nivel de exposición sistémico depende principalmente de los procesos de incorporación (esto es, liberación y absorción) y de eliminación del antibiótico. Efectivamente, el nivel máximo de exposición sistémica al antibiótico administrado mediante una perfusión endovenosa constante (Cpss) y el nivel total de exposición sistémica al antibiótico administrado por vía oral (ABC) son calculados respectivamente de la manera siguiente:
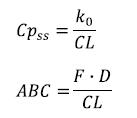
En ambas ecuaciones, el numerador representa el proceso de incorporación del antibiótico: en la primera, k0 es el caudal de perfusión mientras que, en la segunda, F·D es la dosis biodisponible, donde la biodisponibilidad (F) es la fracción de la dosis (D) que alcanza la circulación general tras ser absorbida. El denominador de ambas ecuaciones es el aclaramiento (CL), que es el caudal de eliminación del antibiótico.
Los estudios in vitro, con infecciones experimentales y con ensayos clínicos demuestran que la eficacia antibiótica depende del nivel de exposición sistémico a la droga, respecto al nivel de sensibilidad del agente infeccioso. Esta sensibilidad se mide in vitro con la concentración mínima inhibitoria (CMI). Estos estudios han identificado tres índices de eficacia:

En estos índices, Cmax es la Cp máxima alcanzada tras la dosificación del fármaco y t (Cp>CMI) es el tiempo durante el cual la Cp sobrepasa la CMI. El lector interesado puede referirse a la síntesis bibliográfica de Toutain et al. (2002) para más detalles sobre la relación dosisexposición- efecto antibiótico y sobre la validez de sus indicadores de eficacia.
Es de señalar que en condiciones in vivo, todos estos marcadores están altamente correlacionados entre sí, porque el nivel de exposición sistémica depende no solo de la posología empleada, sino también de las características farmacocinéticas del preparado antibiótico.
Conociendo por una parte la influencia de los procesos de incorporación y de eliminación en la exposición sistémica del antibiótico y, por otra parte, la relación que existe entre la el nivel de exposición al antibiótico, la sensibilidad del agente patógeno a éste y la magnitud del efecto antibiótico que se obtiene, se puede calcular el nivel de dosificación necesario para controlar la infección. Para un antibiótico cuyo índice de eficacia es la razón ABC/CMI, la dosis diaria será:
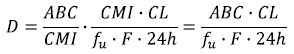
En esta ecuación, el termino fu corresponde a la fracción libre del antibiótico, que debe tenerse en cuenta para ciertas drogas cuya fijación a las proteínas plasmáticas es muy alta (entre otros, ciertas penicilinas, macrólidos y lincosamidas).
DOSIFICACIÓN ORAL DEL ANTIBIÓTICO Y TERAPIA POBLACIONAL
La dosificación de un fármaco en el ganado comprende 6 variables fundamentales: la vía de administración, las condiciones de dosificación, la dosis a administrar, la frecuencia de dosificación, la duración del tratamiento y la duración del periodo de retiro. Puesto que el alimento y el agua son los vehículos más convenientes para el tratamiento poblacional en porcinos, deberemos conseguir que éstos se auto-mediquen de manera que el efecto antibiótico sea de la mayor intensidad en el mayor número de animales posible. Esto se puede conseguir manejando el comedero y el bebedero de manera a que las condiciones, dosis y frecuencia de dosificación no perjudiquen al antibiótico.
Como se ha visto en la última ecuación de este documento, los parámetros farmacocinéticos que determinan la dosis a emplear son el aclaramiento (CL) y la biodisponibilidad (F): cuanto menor sea CL y/o mayor sea F, menor será la dosis a administrar. Estos parámetros son responsables de la ineficacia terapéutica de los aminoglucósidos (por ejemplo, gentamicina) y polipéptidos (por ejemplo, bacitracina) orales en el control de las infecciones sistémicas. Además, el comportamiento alimentario y dípsico de los animales, el sabor del alimento o del agua medicados y el acceso al comedero o el bebedero también determinan la cantidad de antibiótico ingerido, que es lo que últimamente determinará su nivel de exposición sistémico y eficacia antimicrobiana.
El cerdo es un animal cuyo carácter diurno aumenta conforme va llegando a la pubertad. En efecto, el lechón nace con pocas reservas energéticas y amamanta periódicamente durante las 24 horas del día. Los estudios de comportamiento alimentario demuestran que esta periodicidad persiste después del destete y sigue observándose durante la fase de recría: aproximadamente 65% del consumo alimentario diario se realiza durante la fase diurna. En la nave de ceba, el consumo diurno aumenta progresivamente, pasando de unos 70% de la toma diaria una vez que se han aclimatado al nuevo entorno para alcanzar los 85% en las últimas fases de la ceba. Este aumento del comportamiento alimenticio diurno se realiza en paralelo con una disminución progresiva del consumo diario: en la fase de recría el cerdo destetado consumirá diariamente un 5% de su peso vivo (o más, dependiendo del nivel energético y proteico de la ración) para crecer y mantener sus reservas, mientras que en la fase de ceba el consumo pasa del 4% a menos del 3% del peso vivo. El consumo alimentario de las cerdas adultas depende esencialmente del ciclo reproductor: a las cerdas preñadas se les llegará a dar menos del 1.5% del peso vivo para prevenir el síndrome de la cerda grasa, mientras que las cerdas lactantes se les llegará a triplicar la cantidad de alimento servida para que ésta no se debilite amamantando a su camada. Entre los factores que modifican el comportamiento alimentario se destaca la temperatura ambiente, que en verano puede inducir un comportamiento alimentario nocturno, y los niveles dietéticos de energía, proteínas y fibra, que influyen sobre la saciedad.
Esta evolución del comportamiento alimenticio del cerdo hace que para optimizar la eficiencia del tratamiento antibiótico se deba privilegiar a los fármacos con mayor persistencia sistémica (esto es, menor CL) durante las fases de ceba y en animales reproductores adultos. Estos incluyen los macrolidos, fenicoles y tetraciclinas, que tienen entre 5 y 12 horas de vida media. En cambio, en las fases de recría y el inicio de la ceba, cuando el comportamiento alimenticio del cerdo no es tan diurno, se podrán elegir antibióticos como las beta-lactaminas, lincosamidas, tiamulina, sulfadiazina, trimetoprima y, que tienen entre 30 min y 1,5 horas de vida media. La disminución progresiva del consumo diario de alimento del cerdo de engorde trasciende en la eficacia del tratamiento antibiótico cuando éste debe darse durante varias semanas consecutivas.
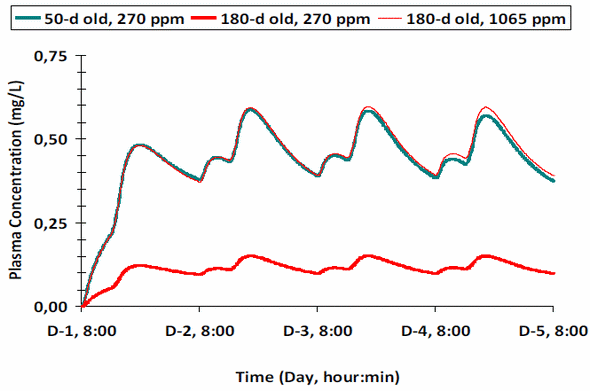
En efecto, nuestros trabajos de investigación han demostrado que el nivel de exposición al antibiótico en la fase de recría disminuye hasta un punto que se deba de aumentar periódicamente el nivel de incorporación en el alimento, con una frecuencia de reajuste proporcional al aclaramiento del fármaco. Esta disminución del nivel de exposición al antibiótico queda patente en la Figura 1: si comparamos las concentraciones plasmáticas de clortetraciclina en cerdos de recría y de final de ceba que ingieren alimentos medicados, el mismo nivel de fortificación de antibiótico producirá en los primeros unas concentraciones plasmáticas 4 veces mayor que en cerdos de ceba. Por tanto, se deberá de aumentar el nivel de fortificación del alimento de cebade manera correspondiente.
El alimento no es un vehículo de administración propicio para las hembras preñadas: por un lado, su alimento está fuertemente racionado durante el embarazo y, por otro lado, se les suele dar de comer una vez al día, lo que impide el mantenimiento de una exposición sistémica eficaz al antibiótico. En cambio, las hembras en lactancia reciben suficiente alimento para que el antibiótico sea eficaz si, y solo si, la frecuencia de comidas es suficiente para mantener una buena exposición sistémica a éste.
Figura 1. Concentraciones plasmáticas medias de clortetraciclina en cerdos de recría, que consumen durante 5 días un alimento fortificado con 270 ppm de antibiótico, y de final de ceba, que consumen un alimento fortificado a la misma concentración o con 1065 ppm de clortetraciclina.
Al contrario del consumo de alimento, el consumo de agua es mucho más constante a través del ciclo de vida del cerdo, no solo en cantidad sino también en frecuencia. Éste beberá entre 8 y 12% de su peso vivo al día, lo que corresponde a sus pérdidas corporales. La temperatura ambiente y la concentración de sodio en el alimento (que está correlacionado al nivel proteico de éste) son los dos principales factores que determinan la variación del consumo de agua. También, un racionamiento excesivo de alimento puede inducir en las cerdas preñadas una toma de agua excesiva (potomanía) para calmar el hambre. Este comportamiento patológico puede tener consecuencias sobre la función renal y la osmolaridad sanguínea.
De cara al tratamiento, la regularidad de la toma de agua permitirá de maximizar la eficacia de todos los antibióticos, especialmente las penicilinas, lincosamidas, sulfadiazina, trimetoprima y tiamulina cuyas persistencias sistémicas son de corta duración. La regularidad de la toma de agua no solo permite aumentar el nivel de exposición sino que también permite mantenerlo con una mayor constancia que el alimento, por lo que su eficiencia terapéutica es mayor que la del alimento. Otra ventaja del agua sobre el alimento es que el antibiótico se ingiere ya disuelto, lo que favorece la absorción y la biodisponibilidad de éste. Los estudios de Wanner en cerdos han demostrado que cuanta mayor sea la humedad relativa del alimento, mayor es la biodisponibilidad de la clortetraciclina, especialmente cuando ésta se incorpora en un alimento con mayor contenido de calcio (como los alimentos para la recría y el principio de engorde).
El mayor problema con el uso del agua como vehículo de administración de antibióticos es que ésta no disimula el amargor que la mayoría de éstos producen. El amargor de antibióticos como las quinolonas y la tilmicosina son suficientes para que los cerdos rechacen el agua medicada. Éstos tienen una gran sensibilidad gustativa, pero los estudios electrofisiológicos demuestran que las sensaciones gustativas de los cerdos no es idéntica a la de los seres humanos. Por ejemplo, el cerdo discierne los azucares simples (que les sabe dulce) de los edulcorantes artificiales (que les son insípidos) mientras que el denatonium, la sustancia más amarga para el ser humano, no es más amarga para el cerdo que la cafeína. Por tanto, es aconsejable de verificar la palatabilidad del agua medicada con los animales y evitar de darles un producto muy amargo a alta dosis, que podría inducir una aversión hacia el vehículo de administración.
Las condiciones de dosificación no se han estudiado mucho en cerdos, salvo el uso de ácidos orgánicos y de suplementos de calcio sobre la biodisponibilidad de las tetraciclinas. Nuestras investigaciones han identificado el nivel de proteínas en el alimento como un posible impedimento para la absorción oral de la amoxicilina. En efecto, la amoxicilina se asemeja a los tripéptidos producidos por la digestión de las proteínas. Es de notar que las proteínas son absorbidas principalmente como como dipéptidos y tripeptidos porque no requiere tanta energía que los aminoácidos. A diferencia de los otros antibióticos, la absorción de la amoxicilina se realiza por medio del trasportador de péptidos, por lo que la distribución de alimentos ricos en proteínas puede disminuir la biodisponibilidad de la amoxicilina. Presentemente estamos investigando el tema para optimizar el uso de este antibiótico de alta importancia en la fase de destete.
Contenido del evento:
Temas relacionados:
Autores:
Université de Montréal, Canada
Recomendar
Comentar
Compartir
Université de Montréal, Canada
10 de marzo de 2014
Estimado Dr Reyes Becerra:
Le agradezco mucho su comentario. También hay que poner en relieve la importancia de una recogida de datos zootécnicos de alta calidad, porque éstos permiten el ajuste de la dosificación a las características de los animales y de su entorno. Por otra parte, estos datos sirven para evaluar la eficacia terapéutica del tratamiento y tomar decisiones en base de la razón coste/eficacia.
Recomendar
Responder
Université de Montréal, Canada
4 de febrero de 2014
Estimado Dr. Henriquez Tejada:
Le agradezco mucho su comentario. Atentamente,
J. del Castillo
Recomendar
Responder
Dinamica del Pacifico
27 de octubre de 2014
Dr. Jerome del Castiillo.
Hoy tuve la oportunidad de ver y leer , su articulo el cual se me hizo de bastante provecho, dejándome claro sus conceptos y aportación, es claro y entendible, y los tomare en cuenta en mi trabajo.
gracias.
Recomendar
Responder
8 de marzo de 2014
Doctor del Castillo es realmente satisfactorio tener la oportunidad de escuchar y leer un articulo tan bien contextualizado. Descripcion sencilla de aspectos farmacologicos y fisiologicos que no son tenidos en cuenta cuando se realizan trabajos de campo.
Recomendar
Responder
Recomendar
Responder

¿Quieres comentar sobre otro tema? Crea una nueva publicación para dialogar con expertos de la comunidad.








.jpg&w=3840&q=75)