Residuos de enrofloxacina y ciprofloxacina en músculo de pollos parrilleros
Las fluoroquinolonas son antimicrobianos de uso intensivo en medicina veterinaria. En Argentina la enrofloxacina es empleada en planteles avícolas y porcinos. La Ciprofloxacina, es un metabolito de la anterior que es empleada en medicina humana y es considerada una alternativa en medicina veterinaria. Niveles de residuos de enrofloxacina y ciprofloxacina se determinaron en forma simultánea en músculo de pollos naturalmente infectados con Mycoplasma spp. y tratados con estos antimicrobianos (5 mg/kg/12h oral) durante 5 días. El objetivo de este trabajo fue establecer el momento adecuado de sacrificio de los animales, para su comercialización en buenas condiciones clínicas y niveles aceptables de residuos. Se sacrificaron animales a cinco tiempos pos-tratamiento; 200 mg de músculo pectoral homogeneizados en buffer fosfato se desproteinizaron, evaporaron y eluyeron por cromatografía líquida de alta presión con detección por fluorescencia. La concentración de residuos de enrofloxacina fue máxima a las 24 h de finalizado el tratamiento (0.073 + 0.006 mg/g), inferior al límite máximo de residuos establecido por entes reguladores internacionales (0.3 mg/g). Los niveles máximos (0.027 + 0.015 mg/g) se detectaron para ciprofloxacina a las 72 h. Es necesario desarrollar y examinar métodos simples y precisos para cuantificar residuos en diferentes productos y tejidos comestibles, promover la aplicación de buenas prácticas agrícolas y elaborar regulaciones pertinentes.
Palabras Clave: micoplasmosis, residuos, fluoroquinolonas, HPLC (cromatografía liquida de alta presión)
Materiales y metodos
Enrofloxacina, base, polvo liofilizado 100% de pureza y Ciprofloxacina clorhidrato, equivalente a 87% de CFX, fueron usados como estandares para el analisis por cromatografía liquida de alta presion (HPLC). Baytril oral, solucion al 10% y Ciprofloxacina clorhidrato fueron empleadas para la administracion de EFX o CFX a los animales. Las soluciones estandares de los antimicrobianos (500 µg/ml de agua deionizada) para estudios de HPLC se prepararon mensualmente. Las soluciones de antimicrobianos para la administración a los animales se prepararon 24 h antes de los ensayos en animales.
El trabajo se llevo a cabo en la Unidad Avicola Experimental de la Facultad de Agronomia y Veterinaria de la Universidad Nacional de Rio Cuarto, con pollos parrilleros provenientes de un establecimiento situado en la zona rural de Rio Cuarto, Cordoba. De un galpon de 5000 pollos parrilleros de la linea COBB con sintomatologia respiratoria se muestrearon 30 animales. Los pollos, de 44 días de edad con 1.73 + 0.15 kg de peso estaban vacunados contra Marek y Gumboro y carecian de tratamiento antibacteriano. Los animales recibieron agua y alimento ad libitum y fueron mantenidos en habitacion cerrada, con pared y piso de cemento, cubierto con cascara de mani. El alimento balanceado fue a base de maiz y sorgo, sin aditivos, ni antimicrobianos. Todos los animales estuvieron sometidos al mismo manejo y los ensayos fueron conducidos sin someterlos a sufrimiento alguno.
Se pesaron 200 mg de musculo pectoral sin aponeurosis. Se homogeneizo cada muestra con 2 ml de buffer fosfato. Los homogeneizados de musculo se desproteinizaron con diclorometano (8 ml), se agitaron manualmente y con vortex 1 min y se centrifugaron a 4000 rpm a 4 oC durante 20 min. Las fases acuosa y organica obtenidas se separaron por filtracion con papel separador de fases, colectando esta ultima. El precipitado se re-extrajo con 6 ml de diclorometano y las fases organicas obtenidas se evaporaron a sequedad a 50 oC bajo corriente de nitrogeno para luego resuspenderlas en 200 µl de fase movil. Las fluoroquinolonas presentes se cuantificaron por cromatografia liquida de alta presion (HPLC), con deteccion por fluorescencia a 295 nm de excitacion y 500 nm de emisiin (8, 9). El ensayo fue lineal desde 0.00375 a 0.1 µg/ml. Los antimicrobianos pudieron ser cuantificados con buena resolucion de ambos picos y ausencia de interferencias por la matriz biologica empleada.
Resultados
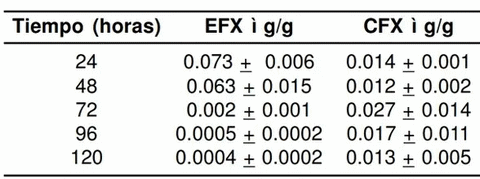
Tabla 1. Residuos de enrofloxacina (EFX) y ciprofloxacina (CFX) en músculo pectoral de pollos parrilleros después de finalizado el tratamiento (24-120 h), con dosis de 5 mg/kg/12h por vía oral durante 5 días
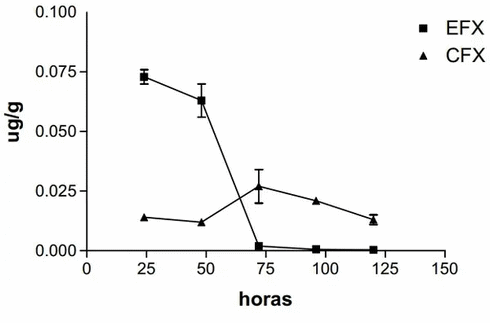
Figura 1. Residuos de enrofloxacina (EFX) y ciprofloxacina (CFX) en músculo pectoral de pollos parrilleros después de finalizado el tratamiento (24-120 h), con dosis de 5 mg/kg/12h por vía oral durante 5 días
1. Abadía AR, Aramayona JJ, Muñoz MJ, Pla Delfina JM, Bregante MA. Ciprofloxacin pharmacokinetics in dogs following oral administration. J. Vet. Med. 1995; 42:501-511.
2. Cerd· O, Xavier JA, Petruccelli MA, Etcheverrigaray ME. Aislamiento de mycoplasma synoviae de pollos parrilleros y gallinas reproductoras. Primera comunicación en la República Argentina. Analecta Vet. 1998; 18(1/2):41-46.
3. Codex Alimentarius: Veterinary Drug Residues in Food-MRL. [ref. de 17 de mayo de 2005 ]. Disponible en Web: http:// faostat.fao.org/faostat/collections
4. Dowling PM, Wilson RC, Tyler JW, Duran SH. Pharmacokinetics of ciprofloxacin in ponies. J. Vet. Pharmacol. Ther. 1995; 18:7-12.
5. FDA. Food and Drug Administration, Center for Veterinary Medicine, Updated Information on FDA ës Proposed withdrawal of Approval of Poultry Fluoroquinolones. [ref. de 17 de mayo de 2005 ]. Disponible en Web:http:// www.fda.gov/CVM/antimicrobial/antimicrobial.HTML
6. GarcÌa Ovando H, Gorla N, Poloni G, Trotti N, Prieto G, Errecalde C. Intravenous pharmacokinetics of ciprofloxacin in goats. Int. J. Antimicrob. Agents. 2000a; 15:77-79.
7. GarcÌa Ovando H, Gorla N, L˚ders C, Poloni G, Errecalde C, Prieto G, Puelles, I. Comparative pharmacokinetics of enrofloxacin and ciprofloxacin in chickens. J. Vet. Pharmacol. Ther. 1999; 22:209-212.
8. GarcÌa Ovando H, Gorla N, Weyers A, Ugnia L, Martinez M, Giacomelli N, Liboa R, Chiostri E, Davicino R. Enrofloxacin liquid-liquid extraction from chicken muscle and HPLC detection. J. Liquid Chromatogr. Rel. Technol. 2000b; 23:2391-2397.
9.- GarcÌa Ovando H, Magnoli A, Gorla N, Weyers A, Ugnia L. Simultaneous quantification of ciprofloxacin, enrofloxacin and balofloxacin in broiler chicken muscle Arch. Med. Vet. 2004; 36 (1):93-98.
10. Gorla N, Chiostri E, Ugnia L, Weyers A, Giacomelli N, Davicino R, GarcÌa Ovando H. HPLC residues of enrofloxacin and ciprofloxacin in eggs of laying hens. Int. J. Antimicrob. Agents. 1997; 8:253-256.
11. Kaneene JB, Miller R. Problems associated with drug residues in beef from feeds and therapy. Rev. Sci. Tech. Off. Int. Epiz. 1997; 16:694-708.
12. Knoll U, Glunder G, Kietzmann M. Comparative study of the plasma pharmcokinetics and tissue concentrations of danofloxacin and enrofloxacin in broiler chickens. J. Vet. Pharmacol. Ther. 1999; 22:239-246.
13. Laguna DS. Residuos de f·rmacos de los alimentos de origen animal. Aspectos regulatorios, analÌticos y toxicológicos, Universidad Nacional de EducaciÛn a Distancia, Córdoba, España, 1995.
14. Mengozzi G, Intorre L, Bertini S, Soldani G. Pharmacokinetics of enrofloxacin and its metabolite ciprofloxacin after intravenous and intramuscular administration in sheep. Am. J. Vet. Res. 1996; 57:1040-1043.
15. Nouws JFM, Mevius DJ, Vree TB, Baars AM, Laurensen J. Pharmacokinetics renal clearance and metabolism of ciprofloxacin following intravenous and oral administration to calves and pigs. Vet. Quart. 1988; 10(3):156-163.
16. Papich MG. Antibacterial drug therapy. Focus on new drugs. Vet. Clin. N. A. Small Animal Practice. 1998; 28(2):215-231.
17. Sato S. La micoplasmosis aviar en Asia. Rev. Sci. Tech. Off. Int. Epiz. 1996; 15(4):1555-1568.
18. Soliman GA. Tissue distribution and disposition kinetics of enrofloxacin in healthy and E.coli infected broilers. Dtsch Tierarztl Wochenschr. 2000; 107:23-27.



Estados Unidos de América







