Rinoneumonitis Equina: un riesgo para la cría y la salud de la población equina colombiana
Publicado: 25 de noviembre de 2005
Por: Julian Ruiz Saenz, MV., MSc. candidato Grupo Inmunovirología, Sede Investigación Universitaria (SIU) Univ. de Antioquia - Medellin, Colombia
La infección por EHV-1 y EHV-4 se caracteriza por una infección primaria en el tracto respiratorio, la cual puede variar de moderada a severa según el estado inmunológico del animal infectado. La infección por EHV-1 particularmente, puede progresar a través de la mucosa respiratoria y llegar a causar abortos en los últimos meses de gestación, muerte perinatal de potros, e incluso sintomatología nerviosa.
En muchas ocasiones la infección primaria por EHV-1 y EHV-4 esta seguida por un estado de latencia viral, en el cual los caballos se encuentran totalmente sanos. Luego de una situación de estrés (transporte, cambio de medio, gestación, etc.) el virus puede reactivarse en estos animales infectados e infectar a otros caballos sanos. Para la identificación de los animales infectados existen gran cantidad de técnicas, siendo la mas apropiada el aislamiento viral, seguida de una confirmación serológica de la entidad.
Durante la infección en el tracto respiratorio, el virus puede aislarse de secreciones nasales; también de muestras de hígado, pulmón, bazo o timo de fetos abortados o de una muestra de sangre tomada al animal en la fase aguda de la enfermedad. Actualmente esta enfermedad se encuentra reportada en el país, sin embargo aún no se toman las medidas necesarias para contrarrestar sus posibles daños, tanto para la industria equina como para la economía nacional.
Introducción
La RE, se diagnosticó por primera vez en el año 1932, año en el cual fue llamada “Aborto Viral Equino”. El virus fue aislado de material de fetos abortados en EE.UU; y su síndrome respiratorio no fue conocido sino hasta mediados de los años 50, cuando el virus fue aislado de secreciones respiratorias de caballos enfermos (1, 7, 22). Aún así, esta enfermedad ha sido reconocida en estudios retrospectivos como causa de aborto en yeguas desde 1921 (25).
En nuestro país, la RE fue reportada finales de 2001, por investigadores de la Universidad Nacional, a partir de un aislamiento viral realizado con base en muestras tomadas de un potro abortado en Bogotá (36). Muchos clínicos sospechan de su presencia en diferentes zonas del país, pero desafortunadamente, no se cuenta con un sistema de vigilancia epidemiológica que permita establecer su verdadera presencia; con el agravante que la mayoría de países vecinos, especialmente Venezuela (7) y Brasil (10,14) poseen reportes y confirmaciones de la enfermedad, además de estar implementando planes de vacunación debido a nuevos brotes (7).
El agente infeccioso (etiología)
Cinco distintos Herpesvirus se reconocen con capacidad de infectar caballos: EHV-4, EHV-1 y EHV-3 (Exantema Coital Equino), los cuales son miembros de la subfamilia Alfaherpesvirinae, y EHV-2 y EHV-5 miembros de la Gammaherpesvirinae. Existen algunos homólogos de EHV-1, EHV-2 y EHV-3, denominados herpesvirus asino-3 (HVA-3), HVA-2 y HVA-1, los cuales han sido aislados de asnos (13,47).
EHV-4 y EHV-1 son Alfaherpesvirus de doble cadena entremezclada de DNA (dsDNA). El genoma completo del EHV-1 se encuentra secuenciado; este posee 150.223 pb, las cuales codifican para proteínas. Se estima que EHV-4 posee 5 kpb menos que EHV-1 (145 kpb). Su reconocimiento como virus distintos se dio en 1981 cuando se demostró que poseían diferentes patrones de restricción de ADN (2,13).
Ambos son grandes causantes de enfermedad respiratoria y abortos respectivamente. En países estacionales se ha dicho que los mayores brotes se presentan durante el invierno y el otoño, conllevando esto a grandes pérdidas económicas a escala nacional e internacional (2, 24,35).
EHV 1-4 han sido aislados de muchas especies de équidos, diferentes a los caballos domésticos, entre ellos asnos, cebras y mulas (1,6) aunque se conoce que los burros poseen mayor resistencia a EHV-1 que los caballos (29). En raras ocasiones se ha reportado la infección EHV-1 en otras especies de animales no équidos como el ganado (aborto), llamas y alpacas (neuropatía del nervio óptico y ceguera) y gacelas en cautiverio (encefalitis) (1).
Epizootiología
Ambos, EHV 1 y 4, son enzoóticos en muchas poblaciones de caballos domésticos. Los virus se desenvuelven en un ciclo ecológico, el cual se desarrolla dentro del caballo, en este se da una persistencia viral postinfección durante toda la vida del animal (estado de latencia) en el cual el virus se encuentra protegido del sistema inmune del animal. Los reservorios epizootiológicos para EHV-1 y EHV-4 son el gran y globalmente distribuido pool de caballos infectados en estado de latencia, los cuales son portadores y diseminadores intermitentes que pueden llegar a infectar más de la mitad de la población equina de un criadero (2).
El ciclo epizootiológico de vida de ambos Herpesvirus es uno solo, el cual consta de tres eventos repetitivos que amplifican y mantienen el reservorio del virus: 1) transmisión intergeneracional (vertical) del virus de la madre al potro, 2) establecimiento del estado de latencia viral posinfección en potros afectados, y 3) reactivación y dispersión periódica del Herpesvirus latente, resultando en una transmisión homo-generacional (horizontal) caballo-caballo.
Dentro de cada caballo el ciclo biológico de EHV-1 y EHV-4 puede describirse como un patrón cíclico de infección: 1) infección, 2) establecimiento de latencia, 3) reactivación periódica de latencia, y 4) diseminación respiratoria (secreciones nasales del reservorio) con transmisión a nuevos hospederos. La mayoría de caballos son infectados durante tempranos estados de vida, convirtiéndose luego en reservorios epizootiológicos. Este ciclo es esencialmente silencioso, con la mayoría de los eventos infecciosos subdiagnosticados como infecciones del tracto respiratorio o con signos tan leves que causan poca alarma (2) (véase Figura 1.)
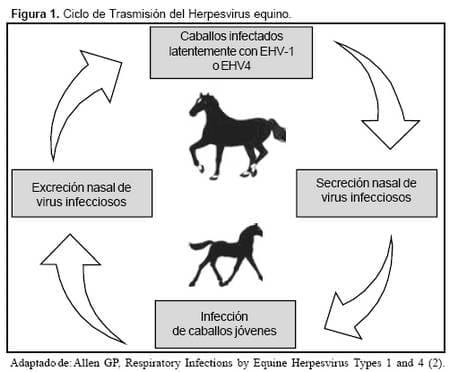
La enfermedad respiratoria causada por EHV-1 o EHV-4 es diseminada de manera más típica entre los caballos jóvenes, con brotes de la enfermedad más comunes en el periodo entre el destete y los dos o tres años de edad (2).
Los factores de riesgo para tales brotes incluyen todas las situaciones que proporcionen estrés a los animales tales como la sobrepoblación, alta carga parasitaria, pobre estado nutricional, climas extremos, y la entrada de animales a diferentes grupos sociales ya establecidos (2).
La transmisión de EHV-1 y EHV-4 en poblaciones susceptibles es muy eficiente, llegando la enfermedad respiratoria a tener una morbilidad del 100%. La RE se presenta comúnmente en un criadero con una tasa de morbilidad clínica baja y una alta prevalencia de infección subclínica demostrable por seroconversión (2).
Tres son los recursos biológicos que pueden servir como origen directo de infección natural para caballos susceptibles:
1. Un caballo infectado activo, el cual libera progenie viral en las secreciones nasales;
2. Los fetos, membranas fetales o secreciones del tracto reproductivo de una yegua, luego de esta haber abortado por EHV (3,44);
3. Y la reactivación endógena del virus del estado latente en el caballo portador (3).
Estudios epidemiológicos conducidos entre 1995 y 2002 en New South Wales, Australia, demuestran que las yeguas son la principal fuente de infección para los potros que aún no han sido destetados (24,26), los cuales, luego servirán para completar el ciclo epidemiológico del virus, diseminándolo a otros potros y permaneciendo como portadores latentes a corta edad de vida, aún antes de realizada una primovacunación, la cual se recomienda entre 5-6 meses de edad (27,28,46). El establecimiento de latencia antes de la vacunación y del destete implica que los potros no creen una buena inmunidad y puedan diseminar el virus a otros grupos de caballos más adelante (28,46).
Latencia
El infectado latente, es un caballo portador crónico de uno o ambos herpesvirus, en el cual el virus persiste subsiguiente a la infección y recuperación de un estado agudo de enfermedad. El porcentaje de caballos portadores asintomáticos es alto; el 60% de los caballos que se recuperan de una enfermedad respiratoria aguda causada por EHV 1-4 se convierten en infectados latentes, los cuales son capaces de transmitir la enfermedad a otros caballos susceptibles por el resto de sus vidas (2).
Los reservorios celulares de esta latencia son las neuronas sensoriales del ganglio trigémino en el caso de EHV-4 (5,42) y de EHV-1 (4,38,42); además, para EHV-1, los linfocitos T del tejido linfoide que drena el tracto respiratorio y el epitelio nasal: ganglios submandibulares, retrofaringeos y nódulos linfoides bronquiales (2,13,35), el nervio olfatorio y el bazo (45). También ha sido reportado en leucocitos de sangre periférica en caballos sin ningún signo clínico de enfermedad (11,40).
En estas células el genoma viral se encuentra presente, sin la producción de partículas virales infecciosas, en un estado de transcripción restringida, en la cual está protegido del reconocimiento y de la destrucción por parte del sistema inmune del animal, y puede mantenerse así por toda la vida del caballo; aún en presencia de una fuerte inmunidad adquirida (2).
El portador latente tiene una importancia crítica para el mantenimiento y la dispersión de EHV 1 o EHV-4, además está estrechamente relacionado con la patogénesis de la enfermedad clínica, debido a su estado reversible. El genoma del virus latente puede reactivarse y comenzar de nuevo con su actividad transcripcional con una consecuente producción de virus infecciosos (2,35)
La reactivación periódica de EHV 1 o EHV-4 está relacionada con episodios de fuerte estrés para los animales, administración de esteroides, cirugías, partos, transportes prolongados, destetes, lactación, disrupción social, etc (2,35). Experimentalmente ambos pueden reactivarse por el uso de prolongadas dosis de corticoesteroides y trauma medio nasal (13).
La reactivación del herpesvirus latente puede ocurrir en ausencia completa de signos clínicos (2). El virus es transportado de manera anterógrada del axón de la célula nerviosa al sitio periférico en el cual se origina la infección, donde causa lesiones recurrentes a través de la replicación viral (5).
El Herpesvirus equino tipo 2 (EHV-2), comúnmente llamado Citomegalovirus equino o herpes de crecimiento lento pueden jugar un importante papel en la reactivación de EHV1 y EHV-4, debido a la inmunosupresión que causa (35).
Signos clínicos asociados a la infección por EHV 1-4
Enfermedad respiratoria
Una enfermedad respiratoria aguda ocurre en animales jóvenes, con mayor frecuencia en el periodo comprendido entre el destete y los 2-3 años de edad (2). Esta es caracterizada por fiebre, letargia, anorexia, linfadenopatía submandibular y descarga nasal profusa, la cual puede llegar a ser mucopurulenta; también es posible encontrar conjuntivitis moderada manifestada por la presencia de secreción ocular (2,13,45). Estos signos pueden ser indicativos de la enfermedad del tracto respiratorio alto, la cual se caracteriza por faringitis y traqueobronquitis con descarga nasal color dorado. Histopatológicamente puede hallarse necrosis extensiva de las células del tracto respiratorio alto, especialmente las de la cavidad nasal, acompañada por una respuesta inflamatoria aguda (2,13,35).
El cambio a una secreción mucopurulenta es el resultado de una infección bacteriana secundaria causada por Streptococcus zooepidemicus . La descarga esta acompañada por tos esporádica. Esta infección es debida a una disminución de la respuesta inmune del animal provocada por el virus o por condiciones externas (35).
El virus puede alojarse en los pulmones generalmente en animales jóvenes y provocar una bronconeumonía exacerbada por la infección bacteriana secundaria con signos de enfermedad respiratoria del tracto bajo como tos, sonidos anormales a la auscultación, incremento en el esfuerzo inspiratorio, etc. (13,35).
En los animales adultos que han estado expuestos a EHV-4 en numerosas ocasiones, los signos clínicos son mínimos, la infección conlleva una reducción en el nivel de productividad del animal, causada por una infección inaparente en el tracto respiratorio alto y bajo (35).
El pronóstico de recuperación completa es bueno y al final de la segunda semana de infección se da una resolución completa de los signos clínicos (2).
Aborto
El más relacionado con episodios de aborto es el EHV-1, el cual causa aborto en yeguas que no muestran ningún signo clínico de enfermedad. Estas generalmente abortan entre los 6 y 11 meses de gestación. El aborto antes de los 5 meses de gestación es raro debido al largo periodo de incubación (9 a 121 días) que requiere el virus (13).
Los tejidos de los potros abortados poseen un amplio rango de lesiones macroscópicas y microscópicas, en los abortos que ocurren a los 6 meses los fetos se encuentran autolisados. En abortos tardíos (luego de 7 meses) hay focos necróticos visibles en aproximadamente el 25% de los casos, en hígado, bazo, pulmones y glándulas adrenales (13).
Los fetos abortados, además de los signos de infección multisistémica presentan altos títulos virales confirmables por el laboratorio (2).
Se han reportado algunas yeguas que abortan luego de 14 a 120 días de la exposición al virus, sin presentar ningún signo clínico (13). Sin embargo, si la infección por EHV-1 es seguida por un estado de latencia viral, podría abortar meses o años después de la infección primaria (13).
La subsecuente eficiencia reproductiva de las yeguas que abortan no es comprometida. El feto abortado el cual no presenta descomposición posmortem, muere a causa de una anoxia provocada por la rápida y progresiva separación placenta- endometrio, la cual precede a la expulsión fetal (2). Los abortos causados por EHV-4 pueden ocurrir, pero con una frecuencia mucho menor que los causados por EHV-1 (2).
Muerte neonatal de potros
Algunos fetos infectados en una etapa terminal de la preñez, pueden nacer vivos y a término, pero enferman al nacimiento o en días siguientes. Los potros se encuentran débiles y requieren cuidados, se presentan letárgicos, piréticos, hipoxémicos y exhiben fuertes deficiencias respiratorias (13,32) . El deterioro clínico en estos potros infectados in útero por EHV-1, ocurre rápidamente y el pronóstico siempre es grave. La mortalidad en estos potros infectados congénitamente es del 100%, debida a una neumonía viral, la cual lleva a una falla respiratoria en unos pocos días. Los potros son altamente susceptibles a las infecciones bacterianas secundarias. La infección congénita por EHV-1 puede ser epizoótica y puede estar relacionada con brotes de abortos por EHV-1. En contraste, raramente se ha asociado a EHV-4 como causa de enfermedad neonatal en potros (2, 13, 45).
Mieloencefalopatía
La mieloencefalitis por herpesvirus es una enfermedad poco común pero devastadora. Se han identificado casos aislados de enfermedad neurológica por EHV-4, pero se presenta generalmente por EHV-1 (2). El intervalo entre la infección inicial del tracto respiratorio y la presentación de los signos neurológicos es de 6 a 10 días. Se presenta principalmente en animales adultos (45) y sus signos neurológicos son variables, la manifestación más común de la enfermedad es la ataxia de los miembros posteriores, la cual progresa hasta la recumbencia (20,41). Algunos caballos pueden presentar parálisis de la pared o el esfínter de la vejiga (2), lo cual conlleva a una incontinencia urinaria (20); algunos pueden presentar inclinación de la cabeza (20). El déficit neuronal resulta de una vasculitis isquémica acompañada de trombosis dentro de los pequeños vasos sanguíneos del sistema nervioso central. Los signos nerviosos aparecen repentinamente, aumentando su intensidad a los 2 ó 3 días y generalmente no son progresivos. El pronóstico de los caballos no recumbentes es favorable, pero es pobre para los animales que permanezcan con sintomatología por más de 2 días (2).
Enfermedad genital
Raramente se ha aislado EHV-1 de enfermedades del tracto genital, y EHV-4 experimentalmente ha producido lesiones en el mismo, ambas similares a las producidas por EHV-3 (Exantema Coital Equino), pero no involucra la piel perineal (13)
Infección vasculotrópica pulmonar
Ha sido reportada recientemente en caballos adultos jóvenes, en casos de enfermedad peraguda generalizada seguida de infección respiratoria. El síndrome denominado “Infección Vasculotrópica Pulmonar por EHV-1”, está caracterizado por fiebre alta, anorexia, depresión severa, dificultad respiratoria y alta mortalidad; los signos neurológicos están ausentes. Los caballos afectados pueden encontrarse muertos. La aparición de la enfermedad es repentina y su progreso a la muerte es rápido. Los hallazgos predominantes a la necropsia, son la vasculitis multisistémica, particularmente prominente en los pequeños vasos sanguíneos de los pulmones (6, 16, 17).
Enfermedad ocular
La infección del tracto respiratorio en potros asociada con cepas hipervirulentas de EHV-1, puede estar acompañada de una seria enfermedad ocular, la cual se manifiesta como una uveitis y/o coriorretinitis (2,21). En casos fuertes, se ha observado extensiva destrucción retinal y ceguera. Los potros lactantes involucrados en casos de brotes de enfermedad neurológica por EHV-1 parecen tener un riesgo particular para esta secuela de la infección (2).
Patología y patogénesis
Enfermedad respiratoria
La RE causada por EHV-4 raramente es fatal. La neumonitis implicada por el nombre es una exageración, ya que en la mayoría de casos la infección es confinada al tracto respiratorio alto y a la tráquea. La muerte neonatal de potros es consecuencia del aumento de la viremia, la dispersión de focos de necrosis en muchos tejidos y órganos, y de neumonía. El número de infecciones fatales aumenta cuando los anticuerpos maternales transferidos al potro son insuficientes o ausentes, y cuando se presentan infecciones bacterianas secundarias. La neumonía es un hallazgo común en estos potros (13).
Después de la infección vía intranasal o por aerosoles, los caballos jóvenes desarrollan distintas lesiones herpéticas en las membranas mucosas a través de todo el tracto respiratorio superior. Hay necrosis del epitelio respiratorio y los centros linfoides germinales, además se puede demostrar la presencia de cuerpos de inclusión intranucleares. Luego de una reinfección, los caballos jóvenes desarrollan una hiperplasia linfoide caracterizada por numerosas figuras mitóticas (13).
Aborto
La ruta natural de infección por EHV-1 es a través del tracto respiratorio superior, seguida por una viremia asociada a células (linfocitos), resultando en una infección placentaria e infección del feto con subsecuente aborto (13).
Los fetos abortados antes de los 6 meses de gestación se encuentran autolisados, es posible encontrar inclusiones intranucleares en células de todo el cuerpo, sin una respuesta inflamatoria celular local
(13). En contraste, las lesiones observadas en los abortos tardíos pueden incluir petequias visibles en las membranas mucosas, edema subcutáneo, exceso de fluido pleural, edema pulmonar, agrandamiento del bazo con prominencia de folículos linfoides y focos de necrosis hepática de un color crema (13,18,34).
Las características microscópicas de las lesiones incluyen bronquiolitis, neumonitis, necrosis severa de la pulpa blanca del bazo y necrosis hepática focal acompañada de una fuerte respuesta inflamatoria celular. En todos los casos las lesiones están asociadas con inclusiones intracelulares herpéticas típicas (13).
Las lesiones en los fetos abortados en etapa temprana de gestación con ausencia de la respuesta inflamatoria celular sugieren la ausencia de respuestas celulares inmunológicas. En contraste, los fetos abortados en estados tardíos, muestran características de respuesta celular. Esto se puede explicar, pues se conoce que el sistema inmune del feto equino es capaz de responder a antígenos específicos a partir de los 7 meses de gestación (13).
Los hallazgos microscópicos en el útero varían de un estado normal, a la presencia de un bajo grado de infiltración perivascular con fuerte infiltración de eosinófilos en el tejido conectivo interglandular del útero. Además, hay completa separación del alantocórion y del endometrio uterino (13). Un estudio de la patogénesis del aborto por EHV-1 en 2001 demostró que se podía encontrar DNA viral en detritos celulares dentro de las glándulas endometriales y que estos se difunden a través de la placenta a sitios de infarto microcotidelonario (39); también se ha podido evidenciar la presencia in vivo del genoma viral en los trofoblastos, sugiriendo una diseminación célula-célula, desde las células endometriales hacia las trofoblásticas (31).
Cuando yeguas preñadas, previamente inmunizadas a EHV 1, son retadas a una reinfección, estas pueden abortar fetos de los cuales el virus no puede ser aislado. La causa del aborto es la dispersa vasculitis, trombosis y daño isquémico secundario al endometrio con replicación de EHV 1 en las células endoteliales. Es común que esos cambios sean la consecuencia de los complejos inmunes específicos al virus que se forman en la vasculatura del endometrio (13).
Muerte neonatal de potros
Las principales lesiones involucran el tracto respiratorio. Los pulmones se encuentran voluminosos y firmes, generalmente de un color “púrpura”, con atelectasis masiva. Se pueden encontrar estriaciones hemorrágicas en la submucosa a lo largo de la tráquea y los bronquios mayores. Los nódulos linfoides bronquiales pueden estar alargados, congestionados y edematosos. Las lesiones microscópicas incluyen alveolitis histiocítica no supurativa y media a severa bronquitis necrotizante focal y/o bronquiolitis con inclusiones intracelulares eosinofílicas. Las lesiones microscópicas del hígado son discretas. Puede presentarse una necrosis adrenocortical focal y disminución y/o degeneración de los linfocitos del timo y del bazo en menos del 50% de los potros. Siempre se encuentran inclusiones intranucleares en los pulmones, frecuentemente en el timo, raramente en el hígado y nunca han sido identificadas en el bazo o glándula adrenal (13,18).
La infección neonatal por EHV-1 causa neumonitis con disminución y/o degeneración de los linfocitos del timo y bazo, la cual facilita las letales infecciones bacterianas secundarias (13). Estos potros tienen la tendencia a tener un conteo total de células blancas menor de 3 x 109 celulas/ml y a encontrarse relativamente ictéricos (33).
Mieloencefalitis
El hallazgo histopatológico de mayor importancia en la mieloencefalitis por EHV es una vasculitis con degeneración hipóxica secundaria en el tejido neural adyacente. Experimentalmente se puede reproducir la condición paralítica con severa vasculitis mediante una inyección subcutánea de EHV-1 cepa Army 183 en yeguas preñadas. Los cambios vasculares son generalmente más prominentes en la médula espinal que en el cerebro (13), mostrando una necrosis hemorrágica espinal (19), y las lesiones en la materia blanca de la médula espinal son más prominentes que las de la materia gris. No se ha reportado evidencia de una infección neurotrópica (inclusiones intranucleares en neuronas, neurofagia, entre otros) (13,41).
Experimentalmente la mieloencefalitis está caracterizada por una vasculitis difusa mas prominente en el tejido nervioso, pero que también afecta endometrio, pulmones y vasos uveales (13).
Durante la viremia asociada a células, en presencia de altos títulos de anticuerpos, el virus puede dispersarse de las células infectadas circulantes directamente a las células endoteliales, contagiando así a estas sin una fase extracelular (13,30). Una vez iniciada la infección endotelial, esta puede diseminarse a través de las células del parénquima adyacente. Esto podría llevar a una severa y generalizada vasculitis sin destrucción neuronal primaria. También se ha sugerido que las lesiones vasculares por EHV-1 son debidas a reacciones inmunológicas específicas para EHV-1 en el endotelio vascular, pues se ha reportado un incremento de cuatro veces los títulos de anticuerpos en caballos con mieloencefalitis por EHV-1 que en caballos expuestos al virus pero sin la enfermedad clínica (13).
Diagnóstico
Debido a las fuertes consecuencias de la infección, es de vital importancia el realizar un certero y rápido diagnóstico. La identificación del agente se puede realizar por diversos métodos, entre estos algunos directos, encaminadas a evidenciar la presencia viral, y otros indirectos, los cuales evidencian la presencia de anticuerpos circulantes contra la entidad. Los segundos no son muy útiles en lugares en los cuales se lleva un régimen de vacunación, pues no es posible diferenciar anticuerpos postvacunales de anticuerpos postinfección (1).
Un definitivo diagnóstico antemortem de la infección por EHV en un caballo, puede ser logrado por aislamiento viral en el laboratorio a partir de muestras de: 1) exudados nasofaringeos colectados en una esponja de dacrón y mantenidos en un medio de transporte líquido o en gel; 2) 15-20 ml de sangre venosa colectada con anticoagulante (EDTA, citrato, heparina). Ambos especímenes para realizar el aislamiento viral, deben ser tomados en tempranos estados de la enfermedad y transportados inmediatamente al laboratorio en estado refrigerado (1,3).
El diagnóstico posmortem puede ser realizado por aislamiento viral, inmunohistoquímica (inmunoperoxidasa), PCR o examinación histopatológica en los tejidos apropiados colectados a la necropsia: pulmones, hígado, bazo y timo de fetos abortados y mortinatos; médula espinal y cerebro en casos de enfermedad neurológica (1,3).
La evidencia serológica de infección reciente por EHV puede ser obtenida por medio del laboratorio a partir de muestras de suero analizadas por fijación del complemento o test de ELISA recombinante. El serodiagnóstico retrospectivo de infección por EHV puede ser demostrado con un aumento en cuatro veces en los títulos virales en muestras de suero de la fase aguda y la fase convaleciente (1).
Los test para diagnóstico han avanzado mucho en la última década, mostrándose como los más apropiados por su rapidez y eficacia los siguientes: el test de fijación del complemento, el cual es muy útil en casos de caballos con parálisis y en casos en los cuales sólo se posea una muestra de suero del estado convaleciente (1,37). Los test de ELISA, los cuales pueden distinguir entre anticuerpos de Herpesvirus equino 1 y 4 y se encuentran comercialmente disponibles (12,48), además existen algunos que distinguen anticuerpos positivos en yeguas asintomáticas preñadas y en neonatos (8). Los test de PCR también son muy usados, son muy rápidos (<8 horas) y sensibles (1,43); al igual que los test de ELISA, algunos pueden distinguir anticuerpo de EHV-1 y 4 y no dependen de la presencia de virus infecciosos en la muestra. Se pueden realizar con muestras de tejidos, de exudados nasofaríngeos, sangre periférica (1,43), algunos test especiales pueden evaluar muestras de semen y embriones (9), muestras de fetos abortados en diversos estados de preservación (23) y detectar animales portadores latentes (10). Un test de PCR- ELISA competitivo desarrollado recientemente, combina las características de ambos y se puede realizar en un solo día, es rápido, sensitivo y facilita el análisis de múltiples muestras (15).
EHV en América y el mundo
En 2001 en Venezuela, la presencia de esta entidad revolucionó al mundo equino a todo nivel, la enfermedad tuvo consecuencias muy graves para la industria equina. En esta epizootia, la presencia del herpesvirus equino fue confirmada por el Laboratorio de Anatomía Patológica de la Universidad Central de Venezuela y el aislamiento del virus se llevó a cabo en Estados Unidos, a partir de muestras de animales que habían enfermado en Venezuela (7).
Según reportes de la OIE, otros países de América que poseen reportes de la presencia del herpesvirus son: Chile, Argentina, Estados Unidos y Canadá, en los cuales el virus se reporta como enzoótico; Brasil lo reporta desde 1994, México desde 1996; en Perú se reporta pero su dispersión se encuentra limitada a algunas zonas del país; en Panamá se tiene reportada y su último brote fue en 1997; en Uruguay se tiene evidencia serológica del agente; y en Paraguay se tiene evidencia de signos clínicos desde 2001, al igual que en la Islas Caimán; en la República Dominicana hay presencia activa del virus desde 1997 hasta a la fecha.
A escala mundial se ha reportado en muchos países con fuerte influencia en la industria equina mundial, como Australia y Nueva Zelanda, en los cuales se encuentra el virus de manera enzoótica; República Checa, Dinamarca, Francia, Finlandia, Alemania, Hungría, Irlanda, Italia, Holanda, Noruega, Polonia, Rumania, Sudáfrica, España, Suecia, Suiza, Reino Unido, Emiratos Árabes, entre otros.
La situación actual de Colombia
En Colombia se logró por primera vez un aislamiento del EHV en Bogotá en 2001, en un laboratorio de la Universidad Nacional de Colombia. El aislamiento viral fue realizado a partir de muestras tomadas de un feto abortado, proveniente de un criadero de equinos, de la zona, el cual tenía historia de importación de animales (36). A parte de este aislamiento, no se tiene ningún estudio que evidencie la verdadera presencia de esta entidad en el país.
La importación de equinos desde otros países es común en muestro medio, siendo ésta una de las principales maneras de introducción del virus al país. En la actualidad Colombia posee vínculos activos de importación de equinos con países en los cuales el herpesvirus equino está presente o se ha reportado, como ejemplo de esto, están las importaciones de caballos criollos argentinos realizadas por la Policía Nacional en 1997 desde Argentina, o la presencia en nuestra ciudad del 6to mundial de caballos de Paso CONFEPASO 2003. Cabe resaltar, que de los 10 países que acompañan a Colombia como miembros de CONFEPASO (Alemania, Suiza, Aruba, Canadá, Panamá, República Dominicana, Curaçao, Puerto Rico, Estados Unidos y Venezuela), el virus está presente o ha sido reportado en ocho de estos.
A pesar de contar con laboratorios de gran influencia y capacidad diagnóstica, y de existir múltiples maneras de realizar un diagnóstico rápido y efectivo, en nuestro país no se realiza este diagnóstico, lo cual hace que tengamos grandes debilidades para lograr controlar esta entidad.
Teniendo en cuenta todos los riesgos y las grandes pérdidas económicas que esta enfermedad acarrea, es necesario que se realicen acciones conjuntas entre el ente público (ICA, Sanidad Agropecuaria etc.), el ente privado (asociaciones de caballistas, criaderos etc.) y las Universidades (entes fuertes en investigación) para desarrollar métodos y técnicas de diagnóstico útiles, rápidas y al alcance de todos, además de sustentar planes de vacunación adecuados a la epidemiología propia; pues de lo contrario, nuestros equinos estarán indefensos ante una enfermedad devastadora para ellos y para la economía, tanto local como nacional.
Agradecimientos
A la Doctora Jenny Jovana Chaparro por su colaboración en la revisión del documento, además al Grupo de Inmunovirología - Biogénesis y al Grupo de Estudio Sobre Equinos
(G.E.S.E.) por su espíritu formador.
Referencias
1. Allen GP, Equine Rinoneumonitis en: Truszczynski M, Pearson JE, Edwards S and Schmitt B, (eds). OIE Manual of standars for diagnostic test and vaccines, 4th edn, OIE press, Paris 2000; 565-575.
2. Allen GP, Respiratory Infections by Equine Herpesvirus Types 1 and 4, In: Equine Respiratory Diseases, Lekeux P. (Eds) International Veterinary Information Service, Ithaca NY, 2002; En: http://www.ivis.org/special_books/Lekeux/ allen/IVIS.pdf (revisado en 2003).
3. Allen GP. Epidemic disease caused by equine herpesvirus-1: recommendations for prevention and control. Equine Vet Educ 2002; 14:136-42.
4. Baxi MK, Efstathiou S, Lawrence G, Whalley JM, Slater JD, Field HJ. The detection of latency- associated transcripts of equine herpesvirus 1 in ganglionic neurons. J Gen Virol 1995; 76:3113-3118.
5. Borchers K, Wolfinger U, Lawrenz B, Schellenbach A, Ludwig V. Equine herpesvirus 4 DNA in trigeminal ganglia of naturally infected horses detected by direct in situ PCR. J Gen Virol 1997; 78:1109-1114.
6. Blunden AS, Smith KC, Whitwell KE, Dunn KA. Systemic infection by equid herpesvirus-1 in a Grevi’s zebra stallion (Equus gevyi) whit particular reference to genital pathology. J Comp Pathol 1998; 119:485-493.
7. Campos G. Rhinoneumonitis equina. Un problema para la cría y la población equina. Venezuela Bovina – Artículos Libres 2001;47: 78-79.
8. Carvalho R, Passos LM, Gouvea AM, Resende M, Martins AS, Franco GC. Use of an ELISA system for detection of equine herpesvirus 1 (EHV-1) antibodies in non-symptomatic pregnant mares and neonatal foals. Arq Bras Med Vet Zootec 2000; 52:200-207.
9. Carvalho R, Passos LM, Oliveira AM, Henry M, Martins AS. Detection of equine herpesvirus 1 DNA in a single embryo and in horse semen by polymerase chain reaction. Arq Bras Med Vet Zootec 2000; 52:302-306.
10. Carvalho R, Oliveira AM, Souza AM, Passos LM, Martins AS. Prevalence of equine herpesvirus type 1 latency detected by polimerase chain reaction. Arch Virol 2000; 145:1773-1787.
11. Chesters PM, Allsop R, Purewal A, Edington N. Detection of Latency-Associated Transcripts of Equid Herpesvirus 1 in Equine Leukocytes but Not in Trigeminal Ganglia. J Virol 1997; 71:3437-3443.
12. Crabb BS, MacPherson CM, reubel GH, Browning GF, Studdert MJ, Drumer HE. A type- specific serological test to distiguish antibodies to equine herpesvirus 4 and 1. Arch Virol 1995; 140:245-258.
13. Crabb BS, Studdert MJ. Equine Rhinoneumonitis (equine Herpesvirus 4) and Equine Abortion (equine Herpesvirus 1) En: Studdert MJ (eds) Virus Infections of Equines. Holanda ELSEVIER 1996; 356.
14. Cunha EM, Ferrari CI, Lara M, da Silva LH. Presença de anticorpos contra o herpesvirus eqüino 1 (EHV-1) em eqüinos do noroeste do estado de são paulo. Arq Inst Biol 2002; 69:1-5.
15. Daly P, Doyle S. The development of a competitive PCR-ELISA for the detection of equine herpesvirus-1. J Virol Methods 2003; 107:237-244.
16. Del Piero F. Pulmonary vasculotropic EHV-1Infection in equids. Vet Pathol 2001; 38:474-475.
17. Del Piero F, Wilkins PA, Timoney PJ, Kadushin J, Vogelbacker H, et al. Fatal nonneurological EHV-1 infection in a yearling filly. Vet Pathol 2000; 37:672-676.
18. Del Piero F, Dubovi EJ. The diagnosis of equine Herpesvirus-1 (EHV-1) abortion and neonatal infection ith enphasis on immunoperoxidase histochemical findings. Vet Pathol 1998; 35:444.
19. Del Piero F, Wilkins PA, deLahunta J, Nelson C, Dubovi EJ. Fifteen cases of equine Herpesvirus-1 (EHV-1) encephalomielopathy in horses: Pathological and immunoperoxidase histochemical findings. Vet Pathol 1998; 35:441.
20. Friday PA, Scarratt WK, Elvinger F, Timoney PJ, Bonda A. Ataxia and paresis with equine herpesvirus type 1 infection in a herd of riding school horses. J Vet Intern Med 2000; 14:197- 201.
21. Gaggl G. Equine Herpesvirus infection. Acase report. Komvet 1998; 2.
22. Galosi CM, Echeverría MG, Vila Roza MV , Cid de La Paz V, Oliva GA, Etcheverrigaray ME. Virus herpes equino tipo 1 (EHV-1): patrones de restricción de ADN, perfiles proteicos y estudio de patogenicidad en ratones. Analecta Veterinaria, 1998; 18:35-40.
23. Galosi CM, Vila Roza MV, Oliva GA, Pecoraro MR, Echeverria MG et al. A polimerase Chain reaction for detection of equine Herpesvirus-1 in routine diagnostic submissions of tissues from aborted foetuses. J Vet Med B Infect Dis Vet Public Health 2001; 48:341-346.
24. Gilkerson JR, Whalley JM, Drummer HE, Studdert MJ, Love DN. Epidemiology of EHV-1 and EHV-4 in the mare and foal populations on a Hunter Valley study farm: are the mares the sourse of EHV-1 for unweaned foals. Vet Microbiol 1999; 65:27-34.
25. Gilkerson Jr, Love DN, Whalley JM. Epidemiology of equine herpesvirus abortion: searching clues to the future. Aust Vet J 1998; 76:675-676.
26. Gilkerson JR, Love DN, Drummer HE, Studdert MJ, Whalley JM. Seroprevalencce of equine herpesvirus 1 in Thoroughbred foals before and after weaning. Aust Vet J 1998; 76:677-682
27. Gilkerson JR, Whalley JM, Drummer HE, Studdert MJ, Epidemiological estudies of equine herpesvirus 1 (EHV-1) in Thoroughbred foals: a review of studies conducted in the Hunter Valley of New South Wales between 1995 and 1997. Vet Microbiol 1999; 68:15-25.
28. Gilkerson JR, Love DN, Whalley JM. Incidence of equine herpesvirus 1 in Thoroughbred weanings on two study farms. Aust Vet J 2000; 78 : 277-278.
29. Gupta AK, Rattan B, Malik P, Kaur D, Sing D Yadav MP. Experimental infection of donkeys whit EHV-1 of horse origin-A study. J equine Sci 2000; 11:29-33.
30. Hasebe R, Kimura T, Nakamura K, Okazaki K, Ochiai K, et al. Passage of equine herpesvirus-1 in suckling mouse brain enhances extraneuronal virus growth and subsequent hematogenous neuroinvasion. J Vet Med Sci 2002; 64:907-912.
31. Mukaiya R, Kimura T, Ochiai K, Wada R, Umemura T. Demostration of equine herpesvirus- 1 gene expression in the placental trophoblast of naturally aborted equine fetuses. J Comp Pathol 2000; 123:119-125.
32. Murray MJ, Del Piero F, Jeffrey SC, Davis MS, Furr MO, et al. Neonatal equine herpesvirus type 1 infection on a thoroughbred-breeding farm. J Vet Intern Med 1998; 12:36-41.
33. Perkins G, Ainsworth DM, Erb HN, Del Piero F, Miller M, et al. Clinical, hematological and biochemical findings in foals with neonatal Equine herpesvirus-1 infection compared with septic and premature foals. Equine Vet J 1999; 31:422-426.
34. Pirarat N, Kiatipattanasakul W, Tharasanit T, Ritruechai P, et al. The detection of equine herpesvirus antigen in an aborted foal using immunohistochemistry: a case report. Thai J Vet Med 2001; 31:57-62.
35. Powell DG. Equine Rinoneumonitis, Equine Rancing 2000; 6:21-23.
36. Ramírez GC, Chaparro JJ, Vera VJ, Villamil LC, Romero JR. Primer aislamiento de herpesvirus equino en Colombia. Rev Col Cienc Pec 2001; 14, sup: 71.
37. Singh BK, Yadav MP, Tewari SC. Neutralizing and complement-fixing monoclonal as an aid to the diagnosis of equine herpesvirus-1 infection. Vet Res Commun 2001,
38. Slater JD, Borchers K, Thackray AM, Field HJ. The trigeminal ganglion is a location for equine herpesvirus 1 latency and reactivation in the horse. J Gen Virol 1994; 75:2007-2016.
39. Smith KC, Borchers K. A study of the pathogenesis of equine herpesvirus 1 (EHV-1) abortion by DNA in-situ hybridization. J Comp Pathol 2001; 125:304-310.
40. Smith SJ, Iqbal J, Purewal A, Hamblin AS, Edington N.In vitro reactivation of latent equid herpesvirus-1 from CD5M/CD8M leukocytes indirectly by IL-2 or chorionic gonadotrophin. J Gen Virol 1998;79: 2997-3004.
41. Stierstorfer B, Eichhorn W, Schmahl W,Brandmuller Ckaaden OR et al. Equine Herpesvirus type 1 (EHV-1) myeloencephalopathy: a case report. J Vet Med B Infect Dis Vet Public Health 2002; 49:37-41.
42. Taouji S, Collobert C, Gicquel B, Sailleau C, Brisseau N, et al. Detection and isolation of equine herpesvirus 1 and 4 from horses in normandy: an autopsy study of tissue distribution in relation to vaccination status. J Vet Med B Infect Dis Vet Public Health 2002; 49:394-399.
43. Varrasso A, Dynon K, Ficorilli N, Hartley CA, Studdert MJ, Drumer HE. Identification of equine herpesviruses 1 and 4 by polymerase chain reaction. Aust Vet J 2001; 79:563-569.
44. Vickers ML, Powel DG. Equnie Herpes Virus abortions. Equine Diseases Quarterly 2001; 10:3.
45. Walker K, Love DN, Whalley M. Comparación od the pathogenesis of acute equine herpesvirus 1 (EHV-1) infection in the horse and the mouse model a review. Vet Microbiol 1999; 98:3-13.
46. Whalley JM, Love DN. Improved vaccine strategies for management of equine herpesviruses. Rural Industries Research and Development Corporation. Sydney, 2002.
47. Wyrick C. Equine Herpesvirus (EHV-4) and 1(EHV-1) Equine Viral Rinoneumonitis en: http:// www.vet.uga.edu/vpp/ia/SRP/ERD/EHV-4 and1.html (revisada en 2003).
48. Yasunaga S, Maeda K, Matsumura T, Kai K, Iwata H, et al. Diagnosis and sero-epizootiology of equine Herpesvirus type 1 and type 4 infections in Japan using a type specific ELISA. J Vet Med Sci 1998; 60:1133-1137.
Temas relacionados:
Autores:
Recomendar
Comentar
Compartir

23 de agosto de 2010
SI BUENOS DIAS PRIMERO QUIERO SABER EN QUE FORO PUEDO HACER LA SIGUIENTE PREGUNTA PUES QUIERO UNA RESPUESTA CONCRETA SOBRE EL CASO QUE VOY A COMENTAR CLARO ESTA QUE SI ALGUIEN DE ESTE FORO LA SABE POR FAVOR COLABORARSE, LA PREGUNTA ES LA SIGUIENTE TENGO UNA POTRA DE AÑO Y MEDIO QUE SE LE HINCHO LA PARTE FRONTAL ARRIBA DE LA NARIZ Y NO PUEDE RESPIRAR BIEN Y ME DICEN QUE ESTO ES POR UNA DESCALCIFICACIÓN Y AQUI A ESA ENFERMEDAD LE DAN LA DENOMINACIÓN DE GALAPAGO Y DICEN QUE ES INCURABLE LA VERDAD QUIERO SABER SI ESO ES CIERTO O QUE CURA TIENE AGRADEZCO A LA PERSONAS QUE SEPAN DEL TEMA COLABORAME. GRACIAS
Recomendar
Responder
6 de agosto de 2010
Cordial saludo Fernando
Si necesitas mas información, envíame un mensaje al correo electrónico julianruizsaenz@gmail.com explicándome cuales son tus ideas iniciales de desarrollo de tesis.
Saludo
Julian
Recomendar
Responder
6 de agosto de 2010
hola doctor julian ruiz
me parece muy valiosa la informacion que proporciona en esta publicacion y en otros articulos referentes al tema que eh encontrado en internet los cuales me demuestra que ud es una de las personas enfocadas a investigar sobre esta enfermedad en el pais.
soy estudiante de la universidad del tolima y eh indagado un poco sobre el tema y me gustaria plantear una tesis o proyecto de investigacion sobre RVE le agradeceria si pudiera colaborarme con el tema. gracias por su atencion.
Recomendar
Responder

20 de junio de 2009
dr Ruiz
lo felicito por su articulo, soy veterinario en popoyan, y ultimamente hemos tenido abortos, motinatos yneonatos con neumonias, de lo cual pienso de estos virus, y no he podido contactar un laboratorio para realizar pruebas directas e indirectas puesto que en algunos criaderos he implementado vacunacion con fluvac.
porfavor si ud. tiene informacion a donde puedo realizar estas pruebas.
gracias
Recomendar
Responder
7 de marzo de 2007
Hola Jennyfer.
Con mucho gusto te renvío información sobre el tema... envíame un correo y yo te reenvío a ese correo los artículos.
Y específicamente, en qué trabajas tu tesis?... para saber qué bibliografía enviarte.
Un Abrazo,
Julian Ruiz Saenz, MV.
Recomendar
Responder

20 de abril de 2006
El manejo inadecuado de los antibióticos así como las vacunaciones en zonas que no son endémicas; y los diagnósticos incompletos hacen que muchas enfermedades se traten como bacteremias, cuando son realmente de tipo viral. Los inmunoestimulantes como el aloe vera y una buena nutrición acompañada de ejercicios diarios, son muy importantes para aumentar los anticuerpos circulantes, y de esta manera nuestros animales puedan defenderse mejor ante virus inmunodepresores.
ATENTAMENTE,
Dr. Giovanni Andrade Heredia
Médico Veterinario UDCA - Colombia
Recomendar
Responder
7 de abril de 2006
Para mí es un gran honor poder presentar este artículo en su revista, pero éste fue publicado previamente en la Revista Colombiana de Ciencias Pecuarias, y por tanto ellos poseen los derechos de publicación. Por tanto el artículo se debe referenciar como:
FUENTE: Revista Colombiana de Ciencias Pecuarias, Vol. 17:2, pág. 156-166, 2004. (Recibido: 29 septiembre, 2003 Aceptado: 17 marzo, 2004).
Disculpen si no es en esta ocasión que puedo contribuir a la revista. De todas formas pudiera escribir una nueva revisión para su revista si la anterior opción no es muy viable.
Julian Ruiz Saenz, DMV, MSc candidato
Grupo Inmunovirología
Sede de Investigación Universitaria (SIU)
Universidad de Antioquia
Medellin, Colombia
Recomendar
Responder

¿Quieres comentar sobre otro tema? Crea una nueva publicación para dialogar con expertos de la comunidad.
Usuarios destacados en Equinos

Jorge Cervantes
Estados Unidos de América

Raul Javier Signorini
Conferencia Internacional de Caballos de Deporte 2012
Médico Veterinario Zootecnista
Estados Unidos de América
Estados Unidos de América
