Contaminación de la castaña y el maní con aflatoxinas
Estudios de contaminación con aflatoxinas producidas por Aspergillus flavus en la castaña y el maní
Las micotoxinas generadas por hongos como Aspergillus flavus y una variedad de hongos se puede hallar contaminando productos alimenticios. Las aflatoxinas liberadas por Aspergillus flavus presente en alimentos producen cáncer en la población que los consume. Se analizaron 40 muestras de castaña y maní por el método microbiológico, 16 muestras dieron cultivo positivo, cuyo desarrollo se observó hasta los diez días. Mediante el ensayo de PCR, 27 muestras dieron positivo para Aspergillus flavus. Se determinó que el maní presenta una mayor contaminación por la aflatoxina producida por Aspergillus flavus. Los factores posibles son, tiempo de exposición y manipulación de éste producto, constituyéndose en un riesgo epidemiológico para la salud de la población. Es vital el control de calidad de estos productos para el consumo humano, con ayuda de la caracterización de estas aflatoxinas mediante herramientas moleculares como la PCR ya que el mismo presenta ventajas en sensibilidad y especificidad frente a los métodos convencionales.
Introducción.
Los hongos se caracterizan por un crecimiento rápido y pueden infectar al hombre, se han descrito aproximadamente 900 especies, siendo 12 las que se relacionan con enfermedades humanas. Aspergillus fumigatus es la especie que produce en mayor porcentaje enfermedades pulmonares, alérgicas e invasivas (85%), Aspergillus flavus con un 5 -10%, Aspergillus níger y Aspergillus terreus con un 2-3%. Estos hongos se encuentran ampliamente distribuidos en el suelo, en la vegetación en descomposición y en una amplia variedad de material orgánico, son patógenos oportunistas que afectan a pacientes inmunocomprometidos.2
En países tropicales se puede hallar a estos hongos contaminando alimentos o productos parcialmente enmohecidos. Según la FAO se estima que el 25% de los cultivos agrícolas a nivel mundial son contaminados por micotoxinas liberadas por los hongos, de las cuales las aflatoxinas son las más importantes1. Las aflatoxinas liberadas por Aspergillus flavus presente en alimentos produce cáncer primario en humanos. El problema de las aflatoxinas se puede presentar en cualquier parte del mundo ya que Aspergillus flavus crece a temperaturas de 25º C y una humedad relativa del 70%. Se pueden hallar en el maíz, cacao, trigo, avena, algodón y otros cereales. 3
El avance de la biotecnología en estos tiempos, nos ha permitido ingresar al uso de técnicas moleculares para el estudio del genoma de Aspergillus, pruebas que requieren de poco tiempo y permiten realizar la identificación de las subespecies de Aspergillus 7. La detección de secuencias especificas de patógenos a través de los métodos moleculares pueden ser herramientas epidemiológicas poderosas para trazar, identificar y controlar fuentes y vías de transmisión e investigar brotes definidos e identificar toxinas particulares.8
En Bolivia, las condiciones de almacenamiento y procesamiento de productos de alimentación son inadecuadas, sobre todo en el oriente y el valle, constituyendo un alto riesgo de contaminación, la escasa higiene en el manipuleo de los alimentos representa un serio problema higiénico sanitario, por la transmisión de las micotoxinas y el hongo, que pueden invadir alimentos almacenados, provocando una disminución en su calidad nutritiva y desencadenando numerosas enfermedades que cursan con cuadros clínicos semejantes, lo que ha veces hace difícil su diagnóstico y notificación. Es imprescindible la correcta identificación del patógeno y el estudio de su patrón de sensibilidad, para controlar y prevenir riesgos epidemiológicos. Creemos que esta intervención contribuirá a frenar a éste patógeno que influye negativamente en el desarrollo social y económico de Bolivia.10
Materiales y Métodos.
Muestras. Se recolectaron 40 muestras (20 de castaña y 20 de cacahuete) con riesgo posible de contaminación por Aspergillus flavus, de regiones productoras de castaña, y maní en las regiones tropicales de Bolivia, (Departamentos: Pando, Beni y La Paz). Se realizó un muestreo del producto en regiones productoras de la castaña, se recolectó de cada muestra aproximadamente 250 gramos (castaña y maní).
Identificación mediante cultivo microbiológico. El aislamiento se realizó en el medio de cultivo Agar Patata Dextrosa (APD). Las muestras procesadas se añadieron por aplicación directa, al medio de cultivo, incubándolo a 25 ºC durante 5 a 7 días, posteriormente se realizó la identificación macroscópica y microscópica.
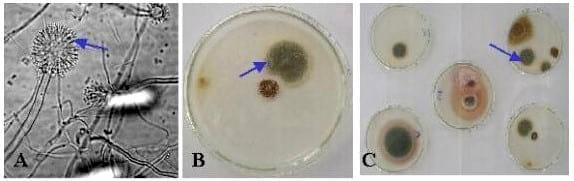
Figura 2. A) Observación microscópica de las conidias de un cultivo de Aspergillus flavus. B) Aislamiento microbiológico en cultivo de una muestra de castaña en medio Agar Patata Dextrosa a los 10 días. C) Aislamiento microbiológico de muestras de maní y castaña, obsérvese la variedad de hongos que desarrollaron.
Identificación mediante PCR.
Aislamiento del DNA. Mediante una lisis se obtuvo el DNA, las colonias de Aspergillus, fueron tratadas con Buffer de lisis (Tris 50mM, pH 7.6, SDS 3%, EDTA 50mM), se incubó a 65 ºC durante 1 hora. Se le añadió cloroformo-TE-fenol en volúmenes iguales y se removió 0,5 ml de la mezcla a otro tubo, añadiéndose fenol-cloroformo el mismo volumen. Se centrifugó a 7500 rpm por 15 minutos. Removiéndose 0,3 ml de la fase acuosa. A la cual se añadió acetato de sodio 3M y alcohol isoamilico, mezclado cuidadosamente, se centrifugó a 7500 rpm por 2 minutos. Se resuspendió el sedimento y fue conservado en TE, a –20ºC.
Reacción en Cadena de la Polimerasa. Para la amplificación por PCR, se empleó: 10X Buffer (100mM Tris pH 8.3; 500mM KCl); dNTPs (10mM c/u); oligonucleotidos (10uM); MgCl2 (25mM); H2O bidestilada; Taq polimerasa (5 U/uL); Glicerol 50%; Aceite Mineral. Cada reacción de 25µl contiene 22.5 µl de la mezcla de PCR y 2.5 µl de la muestra.
La amplificación se realizó en un Termociclador Perkin Elmer 9600, donde el perfil termal aplicado fue: Desnaturalización inicial, 5 minutos; desnaturalización a 94°C por 30 seg, hibridación a 62°C por 1 min, extensión a 72°C por 2 min, esta ronda se llevo por 34 ciclos; una extensión final a 72°C por 10 min, el producto amplificado fue conservado a -4°C. El análisis del producto se realizo mediante electroforesis en geles de agarosa al 2% con Buffer TBE 1X.
Resultados.
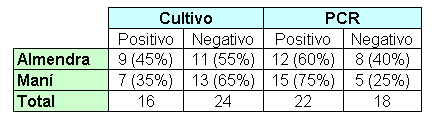
Los medios de cultivo Sabouraud y agar Patata Dextrosa, nos permitieron el aislamiento de diversos hongos, entre ellas cepas de Aspergillus flavus, después de varios días de incubación de las muestras de almendras y maní (cacahuete), se observaron características morfológicas de diferentes tipos de hongos. 40 muestras fueron llevadas a cultivo y de éstas, se pudieron obtener 16 cultivos positivos; el desarrollo se constató en la mayoría de los casos, a los diez días del cultivo. Todas las muestras se incubaron a 25ºC.
La identificación microbiológica de Aspergillus flavus, permitió determinar la mayor contaminación en las almendras en un 45% de las muestras y en el maní en un 35%.
PCR. La amplificación de la región blanco del gen del rRNA 18S altamente conservado en la especie del Aspergillus, lo que hace que a través de ésta técnica se lo pueda tipificar específicamente. De las 40 muestras procesadas por PCR, se observa la amplificación de ADN de Aspergillus flavus en 12 muestras de castaña, lo que representa el 60%. En las muestras de maní en 15 muestras (75%) dieron positivo para A. flavus.
Figura 1. Reacción en Cadena de la Polimerasa (PCR) en muestras de castaña. Electroforesis en Gel de agarosa al 2%, Amplificación de la región blanco del gen del rRNA 18S altamente conservado en la especie del Aspergillus flavus. Línea: 1, control negativo; 2, 3, 4, 5, muestras de castaña; 6, 7, 8, muestras de castaña; 9, control positivo DNA aislado de Aspergillus flavus; 10, Marcador de Peso Molecular de 100 pares de bases. Tamaño del producto 495 pb.
Discusión.
La presencia de aflatoxinas en el presente trabajo es elevado tanto en el maní y la castaña. La toxina se forma cuando estos ubicuos hongos invaden una serie de productos alimenticios, entre los que se incluye la castaña. Lamentablemente, esta nuez constituye un substrato en el cual los hongos producen altos niveles de aflatoxinas y el ambiente en el que se procesa es propicio para la contaminación. Otros productos con problemas de aflatoxinas son: maní, maíz, semilla de algodón, higos, dátiles, almendras y pistacho. También se sabe que ciertas aflatoxinas metabolizadas pueden presentarse en la leche.
Los factores que predisponen a la contaminación son por los hábitos de procesamiento y manipulación antes del consumo humano. La comparación de los resultados obtenidos por el método microbiológico y el ensayo de la Reacción en Cadena de la Polimerasa con respecto a la presencia de Aspergillus flavus en la castaña y el maní, el cual tiene una distribución, que es altamente errática y en pequeños porcentajes del grano de un lote, por lo que es común encontrar altas variaciones en las concentraciones de éste hongo en las muestras representativas de un lote de grano7.
El ensayo microbiológico viene condicionado por los requerimientos de las especies de hongos habituales en los alimentos. La metodología convencional utiliza procedimientos de observación directa, tintoriales y el cultivo, que requiere varios días para detectar y confirmar la presencia del agente causal. Es en este punto donde posiblemente la prontitud diagnóstica pueda tener un especial significado, ya que los resultados positivos tienen una gran repercusión sobre las decisiones que pueden adoptarse, sobre el inicio de medidas de intervención para el control y la prevención de posibles brotes, por lo que un diagnóstico rápido de la presencia del patógeno en una muestra de alimentos se convierte en una prioridad básica de los Servicios de Microbiología. En este sentido, son bien conocidas las limitaciones que el cultivo convencional ofrece, ya que a pesar de que representa el estándar universal, la posibilidad de detección del hongo es reducida, y el tiempo necesario para permitir el crecimiento de estos patógenos es considerablemente largo, ya que al menos deben mantenerse seis días para poder determinar la posibilidad de infección fúngica.
Bibliografía
1. Avise, J.C. (1994). Molecular markers, natural history and evolution. Chapman & Hall, New York. Burke, T. (1992). Spots before the eyes: molecular ecology. Trends in Ecology and Evolution 9: 355-357.
2. RUÍZ HERRERA, José, El asombroso reino de los hongos, Unidad Irapuato del Cinvestav, Avance y perspectiva, Vol. 20.
3. David C., Dimier-David L., Vargas F., Torres M., Dedet J.P. 1993. Fifteen years of cutaneous and mucocutaneous leishmaniasis in Bolivia: retrospective study. Trans. Roy. Soc. Med. Hyg, 87: 7-9.
4. Avise, J.C. (1989). A role for molecular genetics in the recognition and conservation of endangered species. Trends in Ecology and Evolution 4: 279-281.
5. Carvalho, G.R. (1998). Advances in molecular ecology. IOS Press, New York. Dohndt, A.A. (1996). Molecular techniques in conservation and evolutionary biology: a quantum leap?. Trends in Ecology and Evolution 11: 147-148.
6. Albelda, S. M., G. H. Talbot, S. L. Gerson, W. T. Miller, and P. A. Cassileth. 1984. Role of fiberoptic bronchoscopy in the diagnosis of invasive pulmonary aspergillosis in patients with acute leukemia. Am. J. Med. 76:1027–1034.
7. Bodey, G. P., and S. Vartivarian. 1989. Aspergillosis. Eur. J. Clin. Microbiol.
Infect. Dis. 8:413–437.
8. Bretagne, S., J. M. Costa, M. Vidaud, J. Tran Van Hieu, and J. Fleury-Feith. 1993. Detection of Toxoplasma gondii by competitive DNA amplification of bronchoalveolar lavage samples. J. Infect. Dis. 168:1585–1588.
9. Brown, T. A., R. B. Waring, C. Scazzocchio, and R. W. Davies. 1985. The Aspergillus nidulans mitochondrial genome. Curr. Genet. 9:113–117.
10. Cordonnier, C., J. F. Bernaudin, J. Fleury-Feith, M. Feuilhade de Chauvin, C. Haioun, D. Payen, Y. Huet, K. Atassi, and J. P. Vernant. 1985. Diagnostic yield of bronchoalveolar lavage in pneumonitis occurring after allogeneic
bone marrow transplantation. Am. Rev. Respir. Dis. 132:1118–1123.
11. Denning, D. W., S. E. Follansbee, M. Scolaro, S. Norris, H. Edelstein, and D. A. Stevens. 1991. Pulmonary aspergillosis in the acquired immunodeficiency syndrome. N. Engl. J. Med. 324:654–662.
12. EORTC International Antimicrobial Therapy Cooperative Group. 1989. Empiric antifungal therapy in febrile granulocytopenic patients. Am. J. Med. 86:668–672.
13. Fleury, J., E. Escudier, M. J. Pocholle, C. Carre´, and J. F. Bernaudin. 1985.Cell population obtained by bronchoalveolar lavage in Pneumocystis carinii pneumonitis. Acta Cytol. 29:721–726.
14. Hohlfeld, P., F. Daffos, J. M. Costa, P. Thulliez, F. Forestier, and M. Vidaud. 1994. Prenatal diagnosis of congenital toxoplasmosis with a polymerase chain reaction test on amniotic fluid. N. Engl. J. Med. 331:695–699.
15. Hughes, W. T., P. A. Pizzo, J. C. Wade, D. Armstrong, C. D. Webb, and L. S. Young. 1992. Evaluation of new anti-infective drugs for the treatment of febrile episodes in neutropenic patients. Clin. Infect. Dis. 15(Suppl. 1):S206–S215.
16. Kahn, F. W., J. M. Jones, and D. M. England. 1986. The role of bronchoalveolar lavage in the diagnosis of invasive pulmonary aspergillosis. Am. J. Clin. Pathol. 86:518–523.
17. O´Brien, S.J. (1994). A role for molecular genetics in biological conservation. Proc. Natl. Acad. Sci. USA 91: 5748-5755.






Innovaciones en los análisis de aflatoxinas mejoran la calidad de los datos del laboratorio