Introducción
Los bovinos son una de las especies productivas de mayor importancia en el país, por lo tanto, mantenerlos en un adecuado estado de salud es una prioridad para la óptima producción. Sin embargo, existe riesgo constante de contraer infecciones, por lo que, en ese respecto, la prevención de enfermedades juega un papel muy importante y puede mitigarse con varias estrategias. Una de estas es la aplicación de vacunas contra enfermedades infecciosas, siendo un componente principal en el manejo del ganado. No obstante, en ciertas zonas del país, se encuentran presentes patógenos que pueden infectar de por vida a los animales y para los cuales aún no existen vacunas comerciales. Una estrategia más reciente en el diseño de vacunas es el uso de péptidos sintéticos. Esta estrategia se basa en el uso de fragmentos cortos de proteínas para inducir una respuesta inmunitaria muy específica.
Péptidos inmunogénicos sintéticos ante la diversidad de Anaplasma marginale
Uno de los patógeno más importantes para el desarrollo y mejoramiento genético de la ganadería bovina en México, es Anaplasma marginale, la bacteria causante de la anaplasmosis bovina. Este microorganismo infecta las células rojas (eritrocitos) de la sangre de los bovinos, produciendo anemia, pérdida de peso, disminución en la producción de leche, abortos en el último tercio y muerte en bovinos adultos. El principal obstáculo para la generación de una vacuna eficiente a gran escala es que se ha visto que este microorganismo es muy diverso, puesto que, tan sólo en México se han detectado más de 25 cepas de Anaplasma marginale. Con el uso de tecnologías que permiten conocer la secuencia de ADN de fragmentos de genes o genes completos, se han podido observar diferencias entre una cepa y otra, permitiendo la caracterización molecular de 17 de estas cepas, con base en el gen msp1a, así como la secuenciación del genoma completo de 7 cepas de este patógeno del ganado bovino.
Ensayos previos de inmunización con una “vacuna” inactivada mostraron protección al desafío con las mismas cepas que conformaban la vacuna (desafío homólogo o con cepas que compartían una secuencia del gen msp1a), pero que, al desafiar con cepas diferentes (desafío heterólogo o con cepas que no compartían secuencia de msp1a) había una protección parcial. Al mismo tiempo, se realizaron estudios con un candidato vacunal “atenuado” que confería una adecuada protección al desafío homólogo y heterólogo. No obstante, la gran desventaja de este inmunógeno es que se basa en el uso de sangre de bovino, la cual representa un riesgo de transmitir otros patógenos no detectados, además que requiere de transporte en nitrógeno líquido para su óptima conservación y, un manejo y aplicación especializados.
Es por ello que, desde hace algunos años, se han explorado otras alternativas para el desarrollo de vacunas contra la anaplasmosis bovina. Una de estas está basada en el estudio, en primer lugar, de las secuencias de ADN de las múltiples cepas de Anaplasma marginale de las cuales se conoce su genoma. A partir de estas secuencias se realiza la detección de fragmentos correspondientes a proteínas de membrana que se encuentren conservadas (que sean iguales) en las diferentes cepas y, a partir de estas proteínas, se seleccionan fragmentos más pequeños (péptidos) que –idealmente- sean reconocidos por células del sistema inmune. Esos fragmentos, hasta ahora sólo analizados en la computadora, deben enviarse a sintetizar para poder ser usados en ensayos de laboratorio. Así, los péptidos seleccionados de forma virtual con herramientas bioinformáticas, se convierten en un producto tangible: péptidos sintéticos (Figura 1). Estos péptidos sintéticos se deben someter a diversas pruebas de laboratorio para tratar de averiguar si son reconocidos por el sistema inmunitario de los bovinos. No obstante, es necesario también probar en los animales que estos péptidos sean inocuos (que no causen daño al bovino), que sean reconocidos por el sistema inmunitario en condiciones controladas y que, además de ser reconocidos, estimulen a las células inmunitarias a generar una respuesta protectora, con lo cual ya podrían llamarse péptidos inmunogénicos.
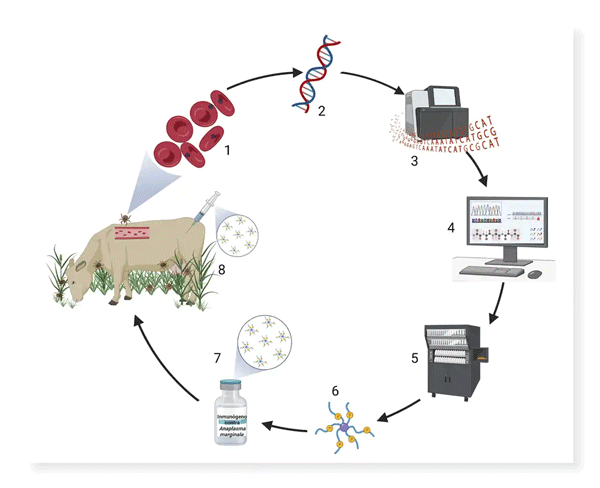
Figura 1. Proceso de generación de un inmunógeno experimental basado en péptidos inmunogénicos sintéticos. 1) A partir de material biológico de un patógeno (en este caso Anaplasma marginale) 2) se extrae el ADN y 3) se obtiene su secuencia genética. 4) Las secuencias son analizadas con herramientas bioinformáticas para encontrar y seleccionar péptidos, 5) los cuales son sintetizados artificialmente 6) en forma de brazos alrededor de una molécula, también llamados Multiple Antigenic Peptides (MAP’s). 7) Estos péptidos son preparados con un adyuvante y posteriormente 8) inoculados en los bovinos a la espera de que desarrollen una respuesta inmune protectora que sea eficiente ante un desafío. (Figura propiedad de la Unidad de Anaplasmosis, CENID-SAI, INIFAP).
Sin embargo, si estos péptidos lograran ser reconocidos y produjeran una respuesta inmune (caracterizada por el desarrollo de anticuerpos y células de memoria), esta respuesta debe ser lo suficientemente fuerte para poder evitar la enfermedad ante una infección real con Anaplasma marginale, y no sólo eso, sino que debe proteger al desafío con diversas cepas de la bacteria, pues de esta forma, ya se podría hablar de un inmunógeno eficaz que pueda usarse a nivel nacional, y con potencial de ser comercializable.
Péptidos inmunogénicos como vacunas para nematodos
Otro ejemplo de patógenos para los cuales sigue siendo complicado el desarrollo de una vacuna comercial eficiente son los nematodos gastrointestinales de los rumiantes. Las infecciones por nematodos representan una amenaza para la salud y el bienestar de los rumiantes en regiones de trópico y clima templado. Todo ganado en pastoreo está expuesto a infectarse; sin embargo, los más susceptibles son los animales jóvenes durante su primera temporada de pastoreo. El uso de antihelmínticos ha sido la opción más frecuente para el control de nematodos durante muchos años, siendo “Barbervax” el único biológico disponible frente a Haemonchus contortus. Sin embargo, en condiciones naturales, las infecciones causadas por estos nematodos no están limitadas a la participación de una sola especie, por lo que la generación de un agente vacunal efectivo debe brindar una amplia protección frente a los parásitos causantes de infecciones mixtas (vacuna multivalente).
Por años, la generación de vacunas frente a nematodos gastrointestinales se ha centrado en el uso de un tipo de proteínas obtenidas principalmente a partir del intestino de los nematodos -mejor conocidas como antígenos ocultos. Estas proteínas son mayormente enzimas nativas (como las serín-proteasas, metaloproteasas, cisteína-proteasas, aspartil-proteasas), así como de otro tipo de proteínas conocidos como productos de excreción y secreción, o como antígenos expuestos. Las enzimas derivadas de intestino han mostrado ser efectivas en la protección de rumiantes, pero poco eficientes en generar memoria inmunológica. Las proteínas de secreción, inducen protección limitada, pero permiten proteger al animal en infecciones secundarias. No obstante, en ambos casos, la obtención a gran escala de estas proteínas a partir de nematodos gastrointestinales para la generación de vacunas podría ser lenta, poco rentable y en algunos casos, imposible de realizar. Por otro lado, las proteínas recombinantes (proteínas generadas en el laboratorio en células distintas a las que las producen normalmente manipuladas para ese propósito) han mostrado ser de menor eficacia protectora debido a la dificultad de mantener las mismas propiedades que sus versiones originales (proteínas nativas), limitando su capacidad de estimular el sistema de defensa del bovino.
Los nematodos son organismos biológicamente complejos por lo que se ha sugerido qué, para estimular una respuesta de defensa adecuada, se requiere: 1) incluir diversas proteínas en una sola vacuna, 2) que éstas estén conservadas, incluyendo antígenos ocultos y expuestos, así como provenientes de diversos géneros de nematodos causantes de estas infecciones. Para ello, gracias a los avances en bioinformática realizados a nivel global, diversas herramientas permiten identificar fragmentos del código genético de los nematodos: ya sea a partir de genomas (la secuencia completa de ADN de un organismo) o transcriptomas (las secuencias completas de productos de los genes generadas por un organismo en determinadas condiciones). Los fragmentos que se buscan son secuencias de péptidos inmunogénicos, porque cuentan con el potencial a ser candidatos vacunales, puesto que son reconocidos por el sistema inmune de los animales o sistema de defensa y pueden desarrollar una respuesta inmunológica que llegue a proteger a los bovinos de las infecciones por estos parásitos. Estos péptidos inmunogénicos podrían ser la clave para sobrepasar las limitantes encontradas con proteínas recombinantes, facilitando el uso de secuencias de diversas enzimas de nematodos gastrointestinales en un solo inmunógeno, y su reconocimiento por el sistema inmune del bovino. De esta manera, la utilización de estos péptidos sintéticos podría permitir el diseño de futuras vacunas multivalentes para nematodos gastrointestinales como Haemonchus sp., Cooperia sp., Oesophagostomum sp., Trichostrongylus sp. y Ostertagia sp en bovinos.
Perspectivas
El desarrollo de vacunas multivalentes a partir de péptidos sintéticos sería altamente benéfico para la salud de los rumiantes susceptibles y para la economía de los productores. Sin embargo, para su propuesta deberá evaluarse la capacidad de estimular el sistema inmune, su reconocimiento por el mismo y la protección brindada a los bovinos ante una infección desafío, controlada y en condiciones naturales.
Se espera que las vacunas basadas en péptidos sintéticos sean la alternativa inocua y eficiente que se ha buscado para controlar las infecciones por nematodos, así como infecciones por hemopatógenos transmitidos por garrapatas como la anaplasmosis bovina, contra la cual se requiere la producción de una respuesta inmune protectora y duradera.
De esta forma se podrían usar como herramienta de prevención y control de enfermedades de los rumiantes, disminuyendo la variabilidad de los lotes de vacunas y potencialmente el número de aplicaciones, facilitando el manejo del inmunógeno.
Publicado originalmente en ganaderia.com








.jpg&w=3840&q=75)