Determinación de la toxicidad de extractos del árbol de paraíso utilizando métodos alternativos al uso de animales de laboratorio
Publicado: 27 de febrero de 2024
Por: Poo J1*, Lenze M2,3., Gerpe MS4, Gutierrez ML2,31INTA Balcarce. 2Inst. de Farmacología, Fac. Med. UBA. 3CONICET. 4IMIIC-CONICET, FCEyN, UNMDP.
Introducción
En la década de 1960 se planteó el concepto de las 3R: remplazo, reducción y refinamiento. Desde ese momento y en especial en los últimos 20 años se han generado esfuerzos tendientes a una menor utilización de animales de laboratorio para el testeo de toxicidad de distintos productos (cosméticos, farmacéuticos, agroquímicos). Bondesson et al. (1989) mostró la correlación de la citotoxicidad en modelos in vitro con la toxicidad oral aguda. La creciente conciencia sobre el sufrimiento y bienestar animal, ha hecho posible la aceptación de la utilización de métodos alternativos en la comunidad científica y organismos regulatorios. De la misma manera y en esa dirección, cada vez son más utilizados los productos naturales como insecticidas o en el tratamiento de enfermedades. La utilización de extractos de Melia azedarach de 10g/dl para el tratamiento de Haematobia irritans (mosca de los cuernos) ectoparásito hematófago de bovinos mostró una eficacia insecticida superior al 90% en ensayos de laboratorio (Poo et al., 2022). Determinar la toxicidad de estos extractos para poder ser aplicados sobre los bovinos es un paso crítico en el desarrollo de un bioproducto. El objetivo de este estudio fue estimar la dosis letal 50 (DL50) de tres extractos de M. azedarach utilizando métodos alternativos, de esta manera se cumple con el reemplazo de animales de laboratorio.
Materiales y Métodos
Los extractos de M. azedarach se elaboraron mediante equipo Soxhlet. Se colectaron frutos, se molieron y se utilizaron 45g para la extracción con metanol, etanol y hexano. Se prepararon los extractos a una concentración de 10g/dl. Para la determinación de la DL50 se utilizó la guía N°129 de la OECD (2010). Brevemente, se utiliza la línea celular BALB/c 3T3 de fibroblastos de ratón, estas se trataron con 8 concentraciones de cada uno de los extractos en 3 ensayos independientes. Las concentraciones fueron de 0,032-100μg/ml en el extracto de fruto etanol (FE), de 0,32- 1000 μg/ml en los extractos de fruto metanol (FM) y fruto hexano (FH). A las 48hs del tratamiento, se determinó la cantidad de células muertas usando la tinción de rojo neutro. A partir de las curvas de cada extracto, se realizó el ajuste no lineal para obtener el valor de CI50 (concentración inhibitoria 50) que corresponde a la concentración que inhibe el 50% de viabilidad celular. Con dicho valor se estimó la DL50 con la siguiente fórmula:
Log (DL50) =0,372*Log (CI50) +2,024
Resultados y Discusión
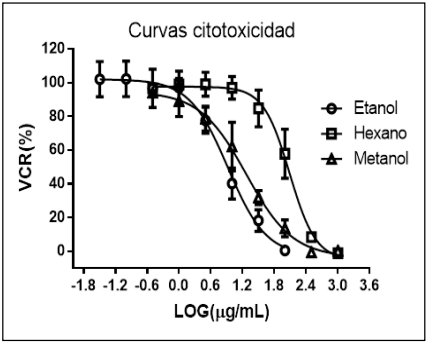
En la Figura 1 se observan las curvas de dosis respuesta de cada uno de los extractos de fruto utilizados. El FE presentó la DL50 más baja con un valor de 232,90mg/kg. Por su parte, FM y FH tuvieron valores de 313,89mg/kg y 631,91mg/kg, respectivamente.
Figura 1. Curvas dosis-respuesta: viabilidad celular relativa (VCR%) vs. Log de la concentración de los extractos (µg/mL). Se representa el promedio y desvío estándar de 3 ensayos independientes. La línea negra corresponde a la regresión no lineal según la función de Hill.
Conclusiones
Los datos de DL50 obtenidos, brindaron información acerca de la seguridad de cada extracto. Conociendo las concentraciones seguras y las concentraciones eficaces para el tratamiento de la mosca de los cuernos, puede planificarse un ensayo clínico piloto a campo garantizando que la aplicación del producto en estudio es seguro. Los resultados alcanzados demuestran que es factible estimar la dosis inicial de la DL50 o la DL50de una sustancia (natural o de síntesis) por una metodología alternativa sin usar animales de laboratorio.
Esta publicación pertenece al 46° Congreso Argentino de Producción Animal
Referencias
Bondesson et al. (1989). Cell. Biol. Toxicol. 5:331-347.
OECD (Organisation for Economic Co-operation and Development) (2010). OECD Series Test Assess, 20: 1-54.
Poo J et al. (2022). XXI congreso ATA. Poster.
Temas relacionados:
Autores:
Instituto Nacional de Tecnología Agropecuaria - INTA
Recomendar
Comentar
Compartir

¿Quieres comentar sobre otro tema? Crea una nueva publicación para dialogar con expertos de la comunidad.




.jpg&w=3840&q=75)