Aflatoxinas B1
Modelo unico in vivo para probar la eficacia de secuestrantes de aflatoxinas B1
Las aflatoxinas son metabolitos secundarios de los hongos, producidos por ciertas especies de Aspergillus, dentro de las cuales B1 es la más perjudicial y la más potente de las micotoxinas que están presentes naturalmente. Las aflatoxinas pueden causar una variedad de efectos, incluyendo pobres desempeños productivos, daño hepático e inmunosupresión. Diversos métodos han sido investigados para reducir la exposición de los animales a las aflatoxinas en alimentos contaminados. La adición de agentes secuestrantes o capturantes en los alimentos balanceados es uno de los más utilizados mundialmente.
Los estudios in vitro utilizados para verificar la capacidad de captura de las micotoxinas son muy útiles para una primera selección de los candidatos potenciales. Sin embargo, es difícil asumir que un producto con una buena eficacia in vitro podría, con certeza, tener un buen desempeño cuando se suministra en el alimento de animales intoxicados. Modelo unico in vivo para probar la eficacia de secuestrantes de aflatoxinas B1.
Material y métodos
Patos (la especie aviar mas sensible a las micotoxinas) fueron seleccionados para el modelo.
Estudio preliminar :
Diseño del protocolo
Dietas contaminadas (50, 125, 250 y 500 ppb) fueron elaboradas adicionando aflatoxina B1 pura sintética a las dietas basales. Patos Pekín de 240 días de edad fueron alojados en 10 jaulas (2 replicas de 24 aves para cada dieta) y alimentados durante 21 días. La mortalidad, pesos individuales y consumo de alimento por jaula fueron registrados semanalmente. Al día 21 de prueba, los animales fueron sacrificados. El peso relativo de sus órganos fue calculado. Parámetros sanguíneos fueron analizados como biomarcadores de intoxicación
Segundo experimento:
Validación del modelo y evaluación del efecto secuestrante protector
En el segundo experimento, el mismo protocolo fue conducido pero con 10 días de duración en lugar de 21. Dos grupos recibiendo 100 ppb de aflatoxina B1 y dos dosis de un secuestrante de aflatoxinas comercial (basado en arcilla) fueron incluidos.
Selección:
Resumen de 15 estudios
Una vez validado, el modelo se utilizó para seleccionar diferentes secuestrantes potenciales (arcillas, extractos de levaduras…etc.) de diferentes regiones del mundo para seleccionar los mas efectivos.
Los resultados del total de los 15 estudios están presentados como resumen de dichas pruebas. Un ejemplo de prueba se detalla en la Tabla 1.
Experimento preliminar :
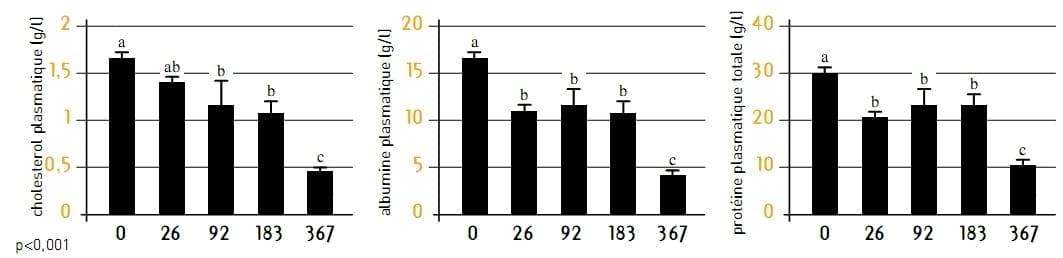
El análisis del contenido de AFB1 de las dietas reveló una contaminación de 26, 92,183 y 367 ppb respectivamente.
mostró tener el más bajo nivel de variación individual y como tal, fue posteriormente correlacionado con otros parámetros plasmáticos (PT/albúmina: r = 0.98 y PT/colesterol : r = 0.9)
La incorporación de 100 ppb de AFB1 durante 10 días ha sido confirmada como la causante de modificaciones significativas en el perfil plasmático. Este efecto fue significativamente contrarrestado por la adición de 5 o 7.5 mg del secuestrante de toxinas de referencia por gramo de dieta contaminada, validando la confiabilidad del modelo para diferenciar y clasificar los productos evaluados por sus efectos protectores contra AFB1 en animales (no se muestran datos).
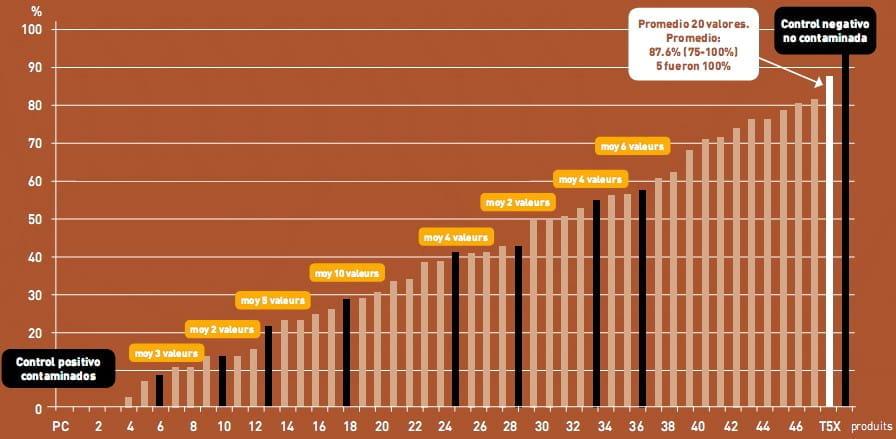
Gráfica 1

15 pruebas incluyendo mas de 20 dietas (250 valores) nos han permitido probar mas de 50 diferentes productos.
El modelo ha permitido identificar los mas eficientes, lo que ha conducido a la creación de T5X. Los ensayos prueban que T5X brinda una replicable y alta protección contra los efectos de la contaminación de aflatoxina B1 En total 20 repeticiones han mostrado que la protección fue de 87.6% en Promedio, con un rango de 75 a 100 % (en 5 pruebas la protección fue de 100%)
Comparación del efecto protector de T5X con diferentes productos comerciales bien conocidos mediante el uso del modelo in vivo de NEOVIA.
CONCLUSIÓN
Pruebas in vitro realizadas en paralelo con pruebas in vivo han mostrado el posible fenómeno de desorción entre pH 3 y 7 (modelización gástrica e intestinal). Diferencias en la clasificación por eficacia se han observado entre los ensayos in vitro e in vivo. Algunos productos con buen desempeño in vitro fallan en nuestro modelo in vivo, confirmando la necesidad de validar los secuestrantes de toxinas in vivo.
- DEVEGOWDA G., T.N.K.MURTHY. 2005. Mycotoxins : their effects in poultry and some practical solutions. The mycotoxin Blue Book. Nottingham University Press 25-56
- JONES,F.T,W.M.HAGLER, and P.B.HAMILTON 1982. Association of low levels of aflatoxins in feed with productivity losses in commercial broiler operations. Poult.Sci.61:861-868.
- RAUBER, R.H.,P.DILKIN, L.Z.GIACOMINI,C.A.A. de ALMEIDA, C.A.MALLMANN 2007. Performance of turkey poults fed different doses of aflatoxins in the diet. Poult.Sci. 86 (8): 1620-1624
- SCHEIDELER S.E., Effects of various types of aluminosilicates and aflatoxin B1 on aflatoxin toxicity, chick performance, and mineral status. Poultry Sci. 1993 72/ 282-288.
Hola Leonel. Mi experiencia en el rubro indica como primera medida evitar los insumos contaminados con aflatoxinas, si tu mismo fabricas tu alimento deberías ser mas fácil,reemplazar los insumos contaminados por insumos aptos y/o alternativos. Para mejorar la condición sanitaria del plantel podrías optar por mejorar el entorno ambiental de las aves mediante sanitizaciones de pabellones y camas de postura, usando un producto natural que no daña a las aves, huevos, ni operadores.
En Chile hemos tenido muy buenos resultados reduciendo la carga microbiana ambiental usando 3 veces por semana un asperjado ambiental con agua electrolizada 25 % disuelta en agua corriente:Mantener baja la carga Microbiana ( hongos y bacterias) reduce las posibilidades de .enfermedades respiratorias sin generar cepas resistentes y con un costo operacional muy reducido.










.jpg&w=3840&q=75)