Elaboración de un Protocolo para el Diagnóstico y Tratamiento de Dermatitis Infecciosas Crónicas en Perros.
Publicado: 8 de agosto de 2014
Por: *Tártara, G. P.; Sarradell, J. E.; Marro, A. V.; Anthony, L. M y François, S. E.
*Fac. de Cs. Veterinarias, UNR, Bv Colón y Bv. Spangemberg, (2170) Casilda, Santa Fe, Argentina.
Resumen.
La dermatitis infecciosa en perros representa un verdadero problema en la clínica dermatológica, ya que en la mayoría de los casos tiende a la cronicidad debido a la instauración de tratamientos empíricos, que culminan en fracasos terapéuticos. Para lograr una adecuada resolución del problema, es necesario recurrir a estudios clínicos complementarios, que permitan revelar cual o cuáles son los factores predisponentes y/o causantes en los perros. Las últimas publicaciones en Dermatología, resaltan la trascendencia del empleo de estudios complementarios, pero no sugieren cuáles serían los principales, ni un orden de aplicación, proceder que consideramos debería existir en forma de protocolo de acción. Los objetivos del trabajo fueron: 1) Identificar el agente patógeno implicado en los casos de dermatitis infecciosas crónicas caninas. 2) Determinar la sensibilidad antibiótica del patógeno aislado y 3) Realizar estudios complementarios para seleccionar aquellos que integren un protocolo de utilidad para el diagnóstico integral y el tratamiento certero de dermatitis infecciosas crónicas.
El agente patógeno aislado de todos los casos analizados fue Staphylococcus intermedius. Los aislamientos fueron sensibles a oxacilina, cefalotina y cefoxitina, con sensibilidad variable a enrofloxacina, amoxicilina más ácido clavulánico, eritromicina y clindamicina, y resistentes en su totalidad a penicilina. Los aislamientos mostraron mayoritariamente resistencia a eritromicina inducible a clindamicina. Los hallazgos histopatológicos corroboraron la existencia de una infección bacteriana. Los análisis clínicos y la ecografía permitieron en algunos casos revelar causas orgánicas subyacentes que no solo predisponen a los animales a padecer cuadros de dermatitis sino que serían responsables de la tendencia a la cronicidad de los mismos. En conclusión, los estudios complementarios utilizados permitieron establecer el diagnóstico y el tratamiento específico para cada caso obteniéndose excelentes resultados clínicos.
Palabras clave: diagnóstico, tratamiento, dermatitis infecciosa, perros, protocolo.
Introducción.
La importancia que las investigaciones en medicina veterinaria adquirieron a lo largo de las últimas décadas, principalmente en clínica de pequeños animales, ha ocasionado un cambio fundamental en los patrones que establecen las bases para el diagnóstico, pronóstico y terapéutica en la práctica médica. La habilidad de trabajar, evaluar críticamente (en relación con su validez y utilidad) e incorporar este creciente cuerpo de evidencias en la práctica diaria, está propiciando un nuevo modelo para la medicina que ha sido denominado “medicina basada en evidencias”. Para poder utilizar este modelo, el médico veterinario debe tener una sólida formación profesional, saber pesquisar, tener acceso a la información actualizada y a los estudios complementarios disponibles, los cuales deberá aplicar e interpretar criteriosamente4.
Existen áreas de la Medicina Veterinaria en la que se instauran tratamientos sin la suficiente evidencia médica y la Dermatología es una de ellas5. Dentro de dicha especialidad, la dermatitis infecciosa en perros es un ejemplo de esta problemática, ya que en la mayoría de los casos tiende a la cronicidad debido a la instauración de tratamientos empíricos, que culminan en fracasos terapéuticos1. El principal agente etiológico bacteriano aislado de lesiones de piel en perros es Staphylococcus intermedius 2,14. Un amplio rango de antibióticos es utilizado para tratar las infecciones dermatológicas causadas por Staphylococcus y su utilización en forma incorrecta ha conducido a la emergencia de cepas resistentes14,16. Debido al aumento de aislamientos de estafilococos resistentes a los betalactámicos, los macrólidos (eritromicina, azitromicina, etc), pueden ser una buena alternativa como tratamiento antimicrobiano. Hasta el presente, son escasos los reportes tanto nacionales como internacionales sobre los mecanismos de resistencia de los estafilococos de origen canino frente a eritromicina3,12. En el mercado se comercializan diferentes productos que incluyen antibióticos de la familia de los macrólidos y dado que estas drogas están estrechamente relacionadas, la determinación de la susceptibilidad in vitro de eritromicina, salvo excepciones, es indicadora de la actividad de los demás macrólidos6.En los últimos años, se comenzó a observar un aumento en la resistencia de S.intermedius frente a los macrólidos7,12,25.
Las dermatitis infecciosas recurrentes de los caninos domésticos suelen deberse generalmente a enfermedades de base como: hipotiroidismo, síndrome de Cushing, alergias, pullicosis, etc, que actúan como factores predisponentes. Por esta razón, para lograr una adecuada resolución del problema, es necesario recurrir a estudios clínicos complementarios, que permitan revelar cual o cuáles son los factores predisponentes y/o causantes en los perros. Se debe pensar, que los tratamientos antibacterianos sistémicos son sólo una parte de la terapia por lo que se constituyen en sólo una parte de la solución, por ello es tan importante que su empleo se establezca criteriosamente y con la mayor precisión posible. Las últimas publicaciones en Dermatología26, resaltan la trascendencia del empleo de estudios complementarios, pero no sugieren cuáles serían los principales, ni un orden de aplicación, proceder que consideramos debería existir en forma de protocolo de acción.
Los objetivos del trabajo fueron: 1) Identificar el agente patógeno implicado en los casos de dermatitis infecciosas crónicas caninas. 2) Determinar la sensibilidad antibiótica del patógeno aislado y 3) Realizar estudios complementarios para seleccionar aquellos que integren un protocolo de utilidad para el diagnóstico integral y el tratamiento certero de dermatitis infecciosas crónicas.
Materiales y Métodos.
Muestras.
Se estudiaron 15 perros provenientes de Clínicas Veterinarias de Rosario. Los animales presentaron dermatitis crónica diseminada con lesiones circulares, escamosas y secas. De cada perro, se analizaron muestras de hisopados y biopsias de la piel lesionada. Para la toma de muestras de piel, se utilizó hisopos estériles humedecidos con agua destilada para lograr una mayor adherencia de las bacterias de la lesión. Se frotó con firmeza sobre los collarines epidérmicos secos. Luego se colocó cada hisopo en medio de transporte de Stuart, para su envío al laboratorio de Microbiología. No se aplicó ningún producto antiséptico sobre el sitio de la lesión, en forma previa a la toma de la muestra.
Para las biopsias, se implementaron los siguientes pasos:
1º Tricotomía y desinfección del área.
2º Se aplico lidocaía al 1% con un atomizador cubriendo el área.
3º Se demarcó el segmento de piel a extraer con fibrón indeleble.
4º A los 5 minutos se aplicó lidocaína al 2% subcutanea, generando un avón.
5º A los 10 minutos se realizó la incisión para extraer muestra.
6º Sutura.
7º La muestra se colocó en formol al 10% para su envío al laboratorio de Histopatología.
2º Se aplico lidocaía al 1% con un atomizador cubriendo el área.
3º Se demarcó el segmento de piel a extraer con fibrón indeleble.
4º A los 5 minutos se aplicó lidocaína al 2% subcutanea, generando un avón.
5º A los 10 minutos se realizó la incisión para extraer muestra.
6º Sutura.
7º La muestra se colocó en formol al 10% para su envío al laboratorio de Histopatología.
Ambos procedimientos fueron realizados sin sedación del animal.
Estudios complementarios.En forma conjunta a cada animal, se le realizó análisis de sangre con hemograma completo, dosaje de urea, creatinina, transaminasas hepáticas, colesterol, triglicéridos y glicemia; ecografía de glándulas tiroides, adrenales, gónadas e hígado. Las muestras de hisopados de piel se sembraron en agar sangre equina al 10% y en agares selectivos de Mc Conkey y Manitol Salado. Se incubaron a 37ºC durante 24 h y las colonias se identificaron mediante pruebas bioquímicas convencionales13. La determinación de la sensibilidad a los antibacterianos se realizó mediante antibiograma por difusión en agar, siguiendo las recomendaciones del Comité Nacional de Estándares de Laboratorios (NCCLS) para patógenos de animales18. Los antibacterianos ensayados fueron: penicilina (peni, 10 UI); cefalotina (cef, 30 µg); cefoxitina (fox, 30 µg); amoxicilina-ácido clavulánico (amc, 30 µg); enrofloxacina (enro, 10 µg); clindamicina (cli, 2 µg) y eritromicina (eri, 15 µg). Se caracterizaron fenotipos de resistencia a macrólidos y lincosamidas, para lo que se utilizó la prueba de doble disco conocida tambien como D-test, colocando un disco de eri a dos centímetros de un disco de cli, según lo recomendado en3,6. Las muestras de biopsias de piel fueron procesadas en el laboratorio de Histopatología por métodos de rutina para hematoxilina y eosina15.
Interpretación de fenotipos de resistencia a eritromicina:
.Fenotipo cMLS (Eri-R y Cli-R): se detectó por la ausencia de un halo de inhibición alrededor de los discos de Eri y Cli, indicando resistencia a ambos antibacterianos.
.Fenotipo iMLS (Eri-R y Cli-S): se detectó por la ausencia de un halo de inhibición frente a Eri y un achatamiento del halo de Cli interpretándose como resistente a ambos antibacterianos.
Resultados.
Del total de las muestras de hisopados de piel analizadas mediante el estudio bacteriológico, se obtuvo Staphylococcus intermedius. La sensibilidad y resistencia a los antibacterianos de los aislamientos obtenidos en este estudio, se muestran en el Cuadro 1. El fenotipo de resistencia a Eri detectado mayoritariamente, se observa en la Fig. 1. El diagnóstico histopatológico de las muestras de biopsias de piel, en todos los casos fue dermatitis perivascular crónica con grados variables de hiperplasia e hiperqueratosis con abundante infliltrado de neutrófilos, estos resultados se observan en las Figuras 2 y 3. Los resultados de los análisis clínicos y estudios ecográficos se muestran en el Cuadro 2.
Cuadro 1. Sensibilidad y resistencia a los antibacterianos de Staphylococcus intermedius aislados de perros con dermatitis crónica
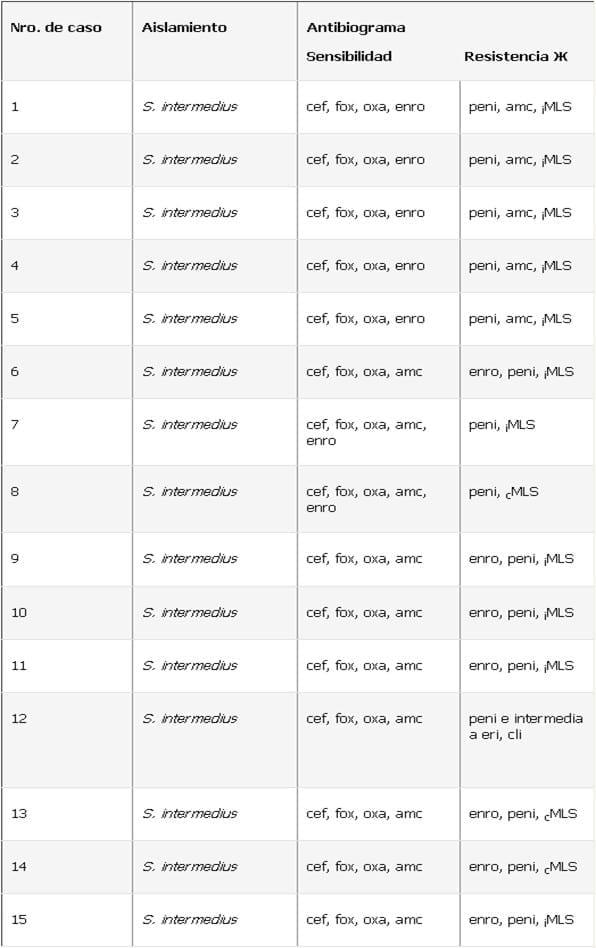 ? iMLS: fenotipo de resistencia a eritromicina inducible a clindamicina.
? iMLS: fenotipo de resistencia a eritromicina inducible a clindamicina.
cMLS: fenotipo de resistencia a eritromicina constitutivo.
 ? iMLS: fenotipo de resistencia a eritromicina inducible a clindamicina.
? iMLS: fenotipo de resistencia a eritromicina inducible a clindamicina.cMLS: fenotipo de resistencia a eritromicina constitutivo.
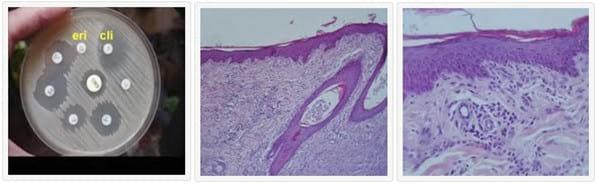 Fenotipo iMLS Hematoxilina y Eosina 10x Hematoxilina y Eosina 40x
Fenotipo iMLS Hematoxilina y Eosina 10x Hematoxilina y Eosina 40xCanino, Mestizo, Macho, 2 años de edad. Dermatitis perivascular hiperplásica con hiperqueratosis.
Infiltrado perivascular de población mixta (mastocitos, escasas célulaslinfoides y polimorfonucleares neutrófilos).
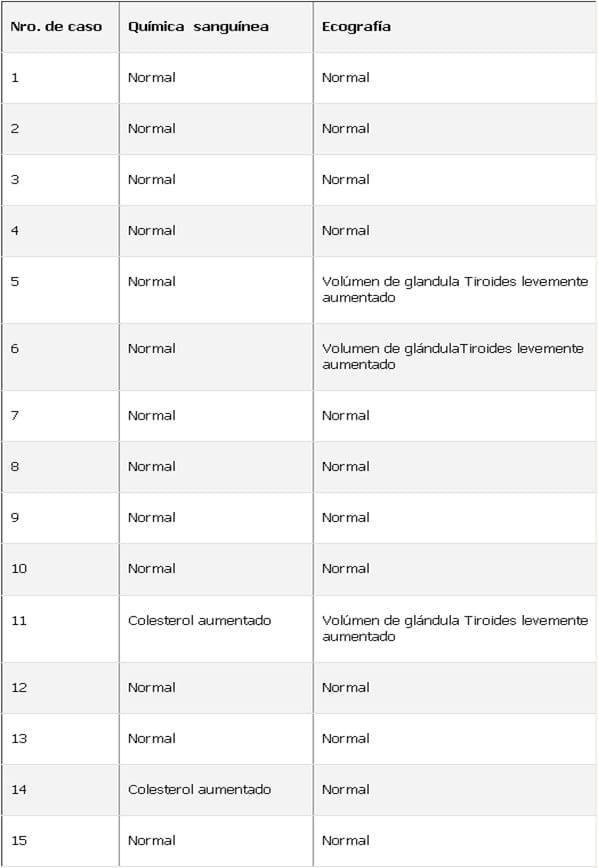
Cuadro 2. Resultados de estudios complementarios realizados en perros con dermatitis crónica.

Discusión y Conclusión.
La toma de muestras mediante hisopado de piel, implementada en este trabajo, resultó eficaz para lograr un análisis bacteriológico adecuado. Los resultados permitieron observar que el principal agente bacteriano aislado de perros con dermatitis crónica esStaphylococcus intermedius, coincidiendo con hallazgos de otros autores a nivel mundial14,16,19. Nuestros hallazgos en cuanto a la sensibilidad a las cefalosporinas de primera generación, que resultaron ser las drogas más eficaces tanto in vitro como in vivo, para inhibir el desarrollo de los aislamientos estudiados, tambien son coincidentes con reportes mundiales9. Los aislamientos de S. intermedius expresaron in vitro, sensibilidad variable a enrofloxacina, coincidiendo con los resultados de otros autores10,24. Los aislamientos mostraron también una sensibilidad variable a amoxicilina en combinación con ácido clavulánico y el más alto porcentaje de resistencia a la penicilina en concordancia con reportes existentes en Brasil22. Nuestro reporte acerca de la expresión de resistencia de S. intermedius de orígen canino a los antibacterianos macrólidos y lincosamidas, es un hallazgo de gran importancia en nuestro país, debido a la escaces de reportes similares en esta especie. Hemos podido observar un fenotipo mayoritario de resistencia a eritromicina inducible a clindamicina en la población estudiada, coincidiendo con reportes de otras partes del mundo12. Es importante desde el punto de vista clínico, detectar in vitro, la resistencia inducible a clindamicina en los aislamientos de Staphylococcus, debido a que existe un potencial desarrollo de resistencia a la droga durante el tratamiento de las infecciones por estos agentes21. Las evidencias mencionadas sugieren que existen diferencias en la resistencia antibiótica de S. intermedius, dependiendo de la región geográfica y de las cepas aisladas. Estos resultados nos permiten concluir, que el estudio bacteriológico de cada caso en particular, así como el antibiograma de los aislamientos obtenidos son estudios complementarios que necesariamente deben integrar cualquier protocolo orientado al diagnóstico y tratamiento de la dermatitis crónica canina.
El diagnóstico histopatológico en todos los casos coincidió con el diagnóstico clínico, indicando un cuadro de dermatitis infecciosa crónica. De esta manera, concluimos al igual que otros autores11, que el estudio histopatológico de biopsias de piel es una herramienta importante para el diagnóstico en Dermatología Clínica.
Los estudios ecográficos y los análisis de la química sanguínea de los pacientes, mostraron en algunas oportunidades, desórdenes de origen endócrino como hipotiroidismo e hipercolesterolemia, que en algunos caninos se presentaron como única alteración metabólica y en otros coincidieron ambos cuadros. Dichos desórdenes, quizás hayan sido las causas responsables de la predisposición de los animales a sufrir un proceso dermatológico crónico. Nuestros supuestos se basan en publicaciones de autores que han demostrado que el hipotiroidismo es la endócrinopatía más común en los perros y es causa de predisposición a infecciones recurrentes de la piel8. También encontramos en determinados casos, caninos que presentaron análisis de química sanguínea y ecografía normales, suponiendo que la dermatitis infecciosa crónica en estos animales, pudo haberse debido a algún estado predisponente que no investigamos, considerando que son numerosas las causas que predisponen a los perros a sufrir dermatitis crónicas23. Al respecto, en el presente estudio descartamos como posibles factores predisponentes la pullicosis o una dieta desordenada, debido a que se instauró una dieta balanceada y un tratamiento antipulgas severo en todos los pacientes estudiados. Desde el punto de vista de las posibles causas subyacentes, el protocolo propuesto aquí es simple, pero permitió arribar a una curación total de cada paciente con excelentes resultados clínicos. En conclusión, los estudios complementarios utilizados, permitieron elaborar un protocolo de acción recomendable a seguir para el diagnóstico y el tratamiento específico de la dermatitis crónica diseminada.
Bibliografía:
1. CARLOTTI, D. N. 2008. Piodermia canina, clasificación anátomo-clínica, terapia y manejo de las formas crónicas. XVIII Simposio Platense de Médicos Veterinarios, Colegio de Med. Vet. de la Plata.
2. CARLOTTI, D. N.; LEROY, S. 1995. Actualités en antibiothérapie cutanée systémique chez le chien. Pract. Med. Chir Anim Comp., 30, 263-271.
3. DENAMIEL, G; MÁS, J.; PUIGDEVALL, T. Y GENTILINI, E. 2004. Resistencia fenotípica a eritromicina en Staphylococcus spp. aislados de infecciones en perros. In Vet, 6(1):29-33.
4. DÍAZ NOVÁS, J.; GALLEGO MACHADO, B. R.; LEÓN GONZÁLEZ, A. 2000. Medicina basada en evidencias. Rev. Cub. Med. Gen Integr., 16(4): 366-9.
5. DRUMMOND, J. P.; SILVA, E.; 1999. Medicina baseada em evidencias. Novo paradigma assistenciale e pedagógico. Atheneu, São Paulo.
6. FAMIGLIETTI, A.; QUINTEROS, M.; PREDARI, S.; CORSO, A.; LOPARDO, H.; CASELLA, J. M.; BANTAR, C.; COUTO, C.; GALAS, M.; GOLDBERG, M., GUDKIN, G.; KOVENSKY PUPKO, J.; MARIN, M.; NICOLA, F.; PASTRERÁN, F.; RADICE, M. 2003. Consenso sobre las pruebas de sensibilidad a los antimicrobianos en cocos Gram positivos. Rev. Arg. de Microbiología, 35: 29-40. ISSN 0325-7541.
7. FRANÇOIS, S.; TÁRTARA, G.; MARRO, A. V.; SARRADELL, J.; ANTHONY, L. 2008. Phenotypes resistant to macrolides in isolated Staphylococcus spp. from canines with dermatitis. Preliminary results. Biocell 32(3), pag. A6.ISSN 0327-9545.
8. FRANK, L. A. 2006. Comparative dermatology-Canine endocrine dermatose. Clin Dermatol., 24(4): 317-25.
9. GANIERE J.; MEDAILLE, C.; MANGION C. 2002. Antimicrobial drug susceptibility ofStaphylococcus intermedius clinical isolates from canine pyoderma. J. Vet. Med. 52: 25-31.
10. GANIERE, J P; MEDAILLE, C; LIMET, A; RUVOEN, N; ANDRE-FONTAINE, G. 2001. Antimicrobial activity of enrofloxacin against Staphylococcus intermedius strains isolated from canine pyodermas.
11. GREGORY, A.; CAMPBELL, M. S.; LESLIE SAUBER. 2007. Getting the most from Dermatopathology. Vet. Clin of North Am. Small Prac. 37 (2): 393-402.
12. GUARDABASSI, L; LOEBER, M E; JACOBSON, A. 2004. Transmission of multiple antimicrobial-resistant Staphylococcus intermedius between dogs affected by deep pyoderma and their owners.
13. HOLT, J. G.; KRIEG, N. R.; SNEATH, P. H. A.; STALEY, J. T.; WILLIAMS, S. T. 1994. Gram positive cocci. In “Brergey´s Manual of Determinative Bacteriology”, Ninth Edition, Williams and Wilkins (eds). Baltimore, Maryland 21202, USA, pp. 544-551.
14. HAUSCHILD, T.; WÓJCIK, A. 2007. Species distribution and properties of staphylococci from canine dermatitis. Res. Vet. Sci, 82(1):1-6.
15. Instituto de Patología de las Fuerzas Armadas de los Estados Unidos de América (AFIP). 1995. “Hematoxilina y Eosina” en: Métodos Histotecnológicos, versión en castellano, edit. y traducida por Clara S. Heffess, M.D; Florabel G. Mullick, M.D. Washington D.C. ISBN 1-881041-21-2.
16. KANIA, S. A.; WILLIAMSON, N. L. ; FRANK, L. A.; WILKES, R. P.; JONES, R. D.; BEMIS, D. A. 2004. Methicilin resistance of Staphylococci isolated from the skin of dogs with pyoderma. Am J. Vet Res., 65(9): 1265-8.
17.LAFORÉ, E. 2006. Evaluación de la tolerancia y efectividad de una formulación a base de amoxicilina más ácido clavulánico (Amoxi-Tab C 250) en la resolución en piodermas en caninos. Internet, disponible en: http://www.agrovetmarket.com/pdf/antibiótico/amoxitabs/pdf.
18. National Comité for Clinical Laboratory Standards. 2002. Performance Standards for Antimicrobial Disk and Dilution Susceptibility test for Bacteria isolated from Animals. Approved Standard. M31-A2, Vol 22, Nro. 6. ISBN 1-56238-461-9.
19. PINCHBECK, L. R.; COLE, L. R.; HILLIER, A.; KOWALSKI, J. J.; RAJALA SCHULTZ, P. J.; BANNERMAN, T. L; York, S. 2006. Genotypic relatedness of staphylococcal strains isolated from pustules and carriage sites in dogs with superficial bacterial foliculitis. Am J. Vet. Res., 67(8): 1337-46.
20. REJAS, J; GONZALEZ, J; ALONSO, P. 1998. Pioderma canina: ¿Qué antibiótico usar?. Peq. Anim. 13: 22-31.
21. RICH, M.; DEIGHTON, L.; ROBERTS, L. 2005. Clindamycin-resistance in methicillin-resistant Staphylococcus aureus isolated from animals. Microbiol, 111: 237-240.
22. SANTOS, M.; AZEVEDO, J.; PETRUCCI, C. 2005. Susceptibilidade a antimicrobianos de bacterias isaladas de diversas patologias em cães e gatos, nos anos de 2002 e 2003. Vet em foco 2:157-164.
23. SCOTT, D. W; MILLER, W. H; GRIFFIN, C. E. 2002. Muller & Kirk`s. Dermatología en pequeños animales. 6ª. Edición. Editorial Inter-Médica S.A.I.C.I. Junín 917, Bs. As.
24. SEOL B. 2005. Comparative in vitro activities of enrofloxacin, ciprofloxacin and marbofloxacin against S. intermedius isolated from dogs.
25. TÁRTARA, G.P.; MARRO, A. V.; SARRADELL, J. E.; ANTHONY, L. Y FRANÇOIS, S. 2009. Resistencia antibiótica de Staphylococcus intermedius provenientes de perros con dermatitis. Libro de resúmenes, pag. 14. V Congreso Bioquímico y 9no. Encuentro Bioquímico, Fac. de Cs. Bioquímicas y Farmacéuticas, UNR, Rosario, 6 de agosto de 2009.
26. Wsava, Congress Proceedings. 2001, 2002, 2003, 2004. Internet. www.wsava.org.
El trabajo fue originalmente publicado en Revista Veterinaria Argentina.
Vet. Arg. – Vol. Nº XXVII – Nº 261 – Enero 2010.
La republicación de los artículos de la Revista Veterinaria Argentina se hace por autorización expresa de Veterinaria Argentina.
*http://www.veterinariargentina.com/revista/2010/01/elaboracion-de-un-protocolo-para-el-diagnostico-y-tratamiento-de-dermatitis-infecciosas-cronicas-en-perros/
Temas relacionados
Autores:
Únete para poder comentar.
Una vez que te unas a Engormix, podrás participar en todos los contenidos y foros.
* Dato obligatorio
¿Quieres comentar sobre otro tema? Crea una nueva publicación para dialogar con expertos de la comunidad.
Crear una publicación24 de marzo de 2015
En realidad mi opinión es para comentar que tengo cuatro labradores retriever los padres dos de color café de 8,5 años de vida y dos hijos de 6,5 años, color caramelo y otro más blanquito, estos últimos me han tenido ya por más de dos años con gastos y gastos, tienen una infección en piel que les produce cuando están más activas muchísima comezon hasta retorcerse cuando uno los acaricia por cualquier región y laceraciones severas porque se rascan o muerden con intensidad; he pasado por muchos Dres. y no mucha ayuda, he llegado por información propia ya que soy Medico de Humanos a tratarlos yo mismo, es así que ahora después de otro fracaso con veterinario decide nuevamente comenzar con prednizona a las dosis recomendadas según el peso y la correspondiente disminución en el tiempo hasta lograr una dosis ideal ya que es lo,que mejor ha pasado parando completamente esa terrible picazon y laceración de la piel.
Son lesiones que comienzan en forma aguda como vesículas planas con color amarillento que luego se seca y queda una forma de costra que al sacarla deja un margen con reborde rojizo y centro más palido que se desprende con todo y pelo dejando parches en toda la piel en forma de apolillado como dice en internet; también están recibiendo cefalexina veterinaria de 500 mg y calculado por el peso, talvez un poco menos cada 12 horas, ya llevamos mas o menos tres semanas e inicialmente mejoraron algo, pero justo hoy que también baja la dosis de la prednizona noto en su piel nuevamente papulas en alas partes posteriores y cuello con forman de costras, hemos estado bañándolos cada semana con shampoo a base de clorhexidina, también toman equilibrium age 1 c/12 horas, comen pepitas de propac súper premium bolsa amarilla mezcladas con pepitas de rico can a base de cordero y remojadas con licuado de higado cocinado, pero no veo grandes resultados, el 17 de Abril se realiza un seminario canino en Quito Ecuador y me voy a inscribir porque necesito hacer algo por mis chicos que se la pasan la mayor parte del tiempo con el collar isabelino tratando de evitar que dañen su piel cuando esto se agudiza; se hicieron hisopados de piel y recuerdo se encontró stafilococus no se si intermedios o decía epidermidis, también debo comentar que hace ya más de dos años al de color caramelo le diagnosticaron de hipotiroidismo y se trató con levotiroxina mejorando espectacularmente, el otro con valores normales. Posterior después de realizar un viaje y dejarlos encargados con un paseador de más perros empeoraron contagiándose todos que nunca había pasado y tuvimos que actuar severamente con baños incluso cada tres días con shampoo llamado broguer-P no recuerdo bien porque la embrida presentó forunculos en las patas y cara con una de ellas muy edema tiznada, disculpen creo me excedí la verdad necesito ayuda para curarlos y verlos felices y mi esposa y Yo igual, gracias por la Paciencia de leer quien lo haga y me sugiera que hacer.



