Introducción
La enfermedad por arañazo de gato (EAG), atribuida originalmente a Chlamydia y virus, se conoce desde hace más de 40 años; sin embargo, su etiología permaneció desconocida hasta los últimos años. Su agente es la bacteria Bartonella henselae, antes llamada Rochalimea henselae (Anderson y Neuman, 1997), que ha sido asociada con diversas enfermedades humanas, además de EAG, como son angiomatosis bacilar, peliosis hepática, bacteremia y endocarditis. El aislamiento de Bartonella henselae aceleró el entendimiento de la epidemiología y patogénesis de estas enfermedades (Slater y col., 1990; Regnery y col., 1992a; Jackson y col., 1993; Anderson y col., 1994; Koehler y col., 1994; Clarridge y col., 1995).
Estudios serológicos y cultivos indican que un alto porcentaje de gatos han estado expuestos o infectados por esta bacteria (Koehler y col., 1994; Childs y col., 1995; Chomel y col., 1995; Jameson y col., 1995). La seroprevalencia varía de acuerdo con la geografía y es influenciada por el clima y probablemente por la presencia del vector (Jameson y col., 1995).
Diversos estudios muestran que los gatos, especialmente jóvenes, son reservorio de Bartonella henselae y su rol en la transmisión de la enfermedad está bien determinado a través de arañazo o mordedura de un gato o de pulga alimentada de un animal infectado. Estos felinos son asintomáticos y no muestran evidencia de la enfermedad. También puede provocar infección ocular si es que se ha acariciado la piel del gato y luego se frota los ojos con la misma mano (Anderson y Neuman, 1997, Maguiña y Gotuzzo, 2000). La historia de contacto con animales, especialmente con arañazo de gato, es clave en el diagnóstico (Simó y col., 1998).
La presencia de Bartonella henselae en Ctenocephalides felis, la pulga del gato, ha sido demostrada (Kirkpatrick y Whiteley, 1987; Kirkpatrick y Glickman,1989; Regnery y col., 1992a; Childs y col., 1994), como también la transmisión experimental de Bartonella henselae de un gato a otro a través de pulgas, siendo propuesta como vector (Chomel y col., 1996; Koehler y col., 1994).
La infección en humanos con Bartonella spp. va desde una linfoadenopatía hasta un compromiso sistémico. La severidad en la presentación de la enfermedad está relacionada con el estado inmune de los afectados (Lucey y col., 1992). Pacientes inmunocompetentes tienden a presentar un cuadro clásico de EAG, mientras que pacientes inmunocomprometidos con SIDA, alcoholismo crónico, inmunosupresión, pueden presentar enfermedad sistémica. (Daly y col., 1993; Hadfield y col., 1993; Spach y col., 1993; Holmes y col., 1995).
Desde que EAG fue descrita en 1950, ésta ha tenido un rápido incremento en el número de casos en el mundo entero. En Estados Unidos se reportan más de 2.000 hospitalizaciones y alrededor de 24.000 casos diagnosticados cada año (Jackson y col., 1993), con una incidencia de 9.3 casos por 100.000 habitantes (Bass y col., 1998; Maurin y Raoult, 1998). El 80% de los afectados son niños con edades entre los 2 y 14 años (Zangwill y col., 1993). El primer diagnóstico en Chile de EAG, fue en noviembre de 1994 y dos años más tarde se publicaron los 10 primeros casos (Abarca,1996). En Valdivia, Navarrete y col en 1999, comunicaron los primeros casos de EAG.
A partir de la identificación de Bartonella henselae como el agente de EAG se desarrollaron técnicas de diagnóstico serológico. La más sensible y específica es la inmunofluorescencia indirecta (IFI). Este examen se ha convertido en la herramienta más útil para el diagnóstico de certeza, evitando la necesidad de realizar biopsia. Recientemente se ha logrado cultivar la bacteria con medios especiales e incubación prolongada. Además, se han desarrollado técnicas de biología molecular para su diagnóstico (Margileth, 1992; Bergmans y col, 1995).
Informamos la detección de Bartonella henselae, mediante técnicas serológicas, en la población felina que concurre al Hospital Veterinario de la Universidad Austral de Chile y otras clínicas privadas de la ciudad de Valdivia, y en los grupos familiares que fue posible, a los cuales pertenecen los gatos seropositivos.
Materiales y Métodos
Obtención de las muestras.
Se obtuvo sangre de una muestra de conveniencia constituida por 76 gatos, mestizos y de raza, de ambos sexos, de tres meses a nueve años de edad, sanos y enfermos de la ciudad de Valdivia, principalmente de la casuística del Hospital Veterinario de la Universidad Austral de Chile (UACh),clínicas veterinarias privadas y de personas que cooperaron voluntariamente. Las muestras fueron recolectadas entre abril y septiembre de 1999. Las muestras de sangre se extrajeron mediante punción de la vena cefálica, safena o yugular y se llevaron al Laboratorio Clínico del Hospital Veterinario de la UACh, donde posteriormente se obtuvo suero, el que fue almacenado en tubos Eppendorf o microtubos a -20ºC.
El número muestral calculado fue de 59 gatos para detectar al menos un individuo seropositivo a Bartonella henselae con un 95% de confianza (Thrusfield, 1995).
Además, se colectó sangre de 22 personas, dueños de gatos que presentaron reacción positiva a Bartonella henselae. La sangre obtenida por punción de la vena cefálica se llevó al Instituto de Microbiología Clínica en la Facultad de Medicina de la UACh, donde se almacenó el suero proveniente de cada una de las muestras en microtubos a _20º C, hasta el momento del análisis.
Recolección de datos.
Mediante anamnesis y examen clínico de los gatos se recopilaron datos sobre edad, sexo, raza, procedencia, actividad (dentro o fuera de la casa) y si presentaban infestación por pulgas. También se obtuvo información acerca de los dueños, para contactarlos posteriormente.
Análisis de las muestras.
Previo al análisis, todas las muestras y los reactivos a utilizar se estabilizaron a temperatura ambiente por espacio de una hora. Se utilizó un sistema de diagnóstico por inmunofluorescencia indirecta de Laboratorios Fuller (USA). Se prepararon diluciones de los sueros a estudiar de 1: 64 y de 1: 256 en PBS. En cada "pocillo slide" con células Vero infectadas con Bartonella henselae, se colocaron 10 ml. de cada dilución (1: 64 y 1: 256 respectivamente). Por cada ensayo se incluyó una dilución del control positivo y negativo. Se siguieron las pautas del fabricante. Seguidamente se observó a 400x en microscopio de inmunofluorescencia buscando bacilos pleomórficos en el citoplasma de las células Vero, con fluorescencia intensa de color verde manzana. Fueron consideradas positivas aquellas muestras en que se observaba fluorescencia en ambas diluciones, dando como punto de corte el título 1: 64. En aquellas en que la dilución 1: 256 era negativa y débil en el título 1:64 fueron dadas como negativas.
Análisis estadístico.
En la comparación de las prevalencias serológicas se utilizó la prueba de chi cuadrado con un nivel de significación de 0.05.
Resultados y Discusión
Se estudió un total de 76 gatos, de los cuales 54 (71%) resultaron seropositivos a Bartonella henselae por la prueba de inmunofluorescencia indirecta. En 26 (68.4%) de los 38 (50.0%) machos muestreados se detectó la presencia de anticuerpos contra Bartonella henselae, en cambio, en 28 (73.7%) de las 38 (50.0%) hembras investigadas se obtuvieron resultados positivos a la reacción. No se encontraron diferencias significativas (p<0.05) entre la proporción de gatos positivos según sexo.
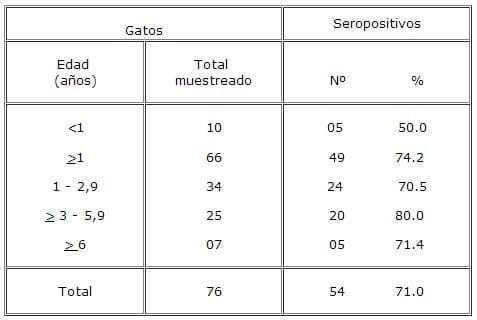
La distribución de los seropositivos según edad se muestra en el cuadro 1. Las mayores seroprevalencias se encontraron en los gatos de 3 a 6 años de edad. Al compararse la proporción de gatos seropositivos menores y mayores de un año de edad, la diferencia no fue significativa (p<0.05).
CUADRO 1. Prevalencia de anticuerpos contra Bartonella henselae , según edad, en 76 gatos de la ciudad de Valdivia, Chile.
Bartonella henselae antibody prevalence by age among 76 cats from the city of Valdivia, Chile.
De los 42 (58.3%) gatos que permanecían la mayor parte del tiempo dentro de la casa, 29 (69%) resultaron seropositivos. Por el contrario, de los 34 (44.7%) gatos que pasaban la mayoría del día fuera de la casa, 25 (73.5%) resultaron seropositivos. No se encontraron diferencias significativas en la proporción de gatos positivos que se encontraban dentro y fuera de la casa (p<0.05).
Al examen clínico, 67 (88%) animales presentaron pulgas, de éstos, 50 (75%) resultaron positivos a la reacción. En los 9 (12.0%) animales sin evidencia clínica de pulgas, en 4 (44%) de ellos se detectaron anticuerpos contraBartonella henselae. No se encontraronó diferencias significativas entre la proporción de gatos positivos según presencia de pulgas (p<0.05).
De 22 personas estudiadas, dueñas de gatos seropositivos, en 4 (18.0%) se encontraron anticuerpos contra B. henselae, dos de ellas de sexo masculino (de 74 y 66 años) y dos mujeres (de 32 y 22 años de edad).
Bartonella henselae ha sido reconocida como causante de la enfermedad por arañazo de gato y angiomatosis bacilar y su espectro clínico se está aún expandiendo. Los gatos son, hasta ahora, el único reservorio conocido de B. henselae (Koehler y col., 1994). Diversos investigadores han informado de una alta seroprevalencia y de una bacteremia asintomática por B. henselae entre poblaciones de gatos naturalmente infectados (Zangwill y col., 1993; Koehler y col., 1994; Breitschwerdt y Kordick, 1995; Childs y col., 1995; Chomel y col., 1995; Jameson y col., 1995; Kordick y col., 1995; Ueno y col., 1995; Von Allerberger y col., 1995).
En el presente estudio, en gatos de Valdivia, la seroprevalencia para Bartonella henselae, fue de un 71%.
El porcentaje de seropositivos hallados es visiblemente mayor al observado en otros continentes; por ejemplo en Europa, Bergmans y col. en 1996 encontraron una seroprevalencia de 50% en gatos en Holanda; a su vez Von Allerberger y col. (1995) informaron de 33% de seropositivos en Austria. En Francia se encontró B. henselae en un 11% de los gatos (Clarridge y col., 1995; Lawson y Collins, 1996). En Japón, Ueno y col. (1995), describen una seroprevalencia de 15.1% en gatos domésticos, mientras que en Norteamérica, Koehler y col. (1994) comunicaron una prevalencia de 41% en gatos del área de la bahía de San Francisco.
Las menores seroprevalencias encontradas en otros países podrían explicarse por el promedio de temperatura y humedad que hay en esos lugares que no serían los más apropiados para el desarrollo y multiplicación del vector. En cambio, si se compara el resultado de este estudio con el 81% encontrado por Chomel y col. (1995) en gatos de California, se observa que éste es ligeramente menor. Esto puede ser explicado por el hecho de que de los 205 gatos que ellos muestrearon, 44 estaban altamente infestados por pulgas y todos pertenecían al mismo dueño. Todos estos gatos tenían anticuerpos contra Bartonella henselae. Si el resultado de estos 44 gatos fuera omitido, se obtendría una seroprevalencia de 76%, la que estaría más cercana a la determinada en el presente trabajo.
Esto indicaría que tanto en California como en Valdivia se encontrarían las condiciones necesarias para la permanencia y multiplicación del vector en el medio. Si se compara con los escasos estudios nacionales,en otras ciudades dentro de Chile, se puede ver que la seroprevalencia encontrada en Valdivia es muy similar a la de la ciudad de Coquimbo, la cual fue de 79.2% y es bastante menor si se compara con los gatos muestreados en la región Metropolitana que fue de 96%, en que la mayoría de los animales eran vagabundos (87%) y el 80% de ellos presentaba gran cantidad de pulgas (Ferres , 2000*).
Detectamos una mayor proporción de hembras seropositivas (73.7%) en relación a machos (68.4%); esta leve diferencia existente difiere de lo encontrado por Bergmans y col. (1996) en Holanda que arrojó un porcentaje de seropositividad levemente mayor en machos (55%) sobre las hembras (47%). Al parecer estos autores son los únicos que informan esta diferenciación.
La alta seropositividad encontrada en gatos adultos (mayores de un año) que varía desde un 71% a un 80%, en comparación con el 50% de reaccionantes encontrados en gatos menores de un año de edad, concuerda con lo informado por Bergmans y col. (1996) en gatos de Holanda, que fue de 40% para gatos menores de un año y entre 50 a 58% de seropositivos para gatos mayores de un año; sin embargo, contrasta con lo reportado porChomel y col. (1995) en California, quien señala un porcentaje de 90.7% de animales seropositivos dentro del grupo de menores de un año y un promedio de 76% para gatos adultos.
En Chile, en la región Metropolitana, se informa que la mayoría de los gatos seropositivos (74%) correspondió a animales mayores de un año de edad. No se encontraron diferencias significativas entre gatos mayores y menores de un año, destacando que el número de los felinos menores de un año fue bajo. Esto concuerda con lo encontrado en Coquimbo, en que un 75% de los gatos reaccionantes eran mayores de un año de edad (Ferres, 2000*)
*Comunicación personal: Lab. de Infectología y Virología Molecular, Universidad Católica de Chile, Chile.
En este estudio no se encontraron diferencias significativas entre los animales mayores y menores de un año de edad, pero hay que señalar que el número de gatos muestreados para la categoría de menores de un año fue bajo, lo cual pudo determinar que no se alcanzara una diferencia estadística significativa. De los animales muestreados en Valdivia el porcentaje más alto de seropositivos se encontró en el grupo de gatos de 3 o más años y menos de 6 (80%).
Los animales en estudio se dividieron en dos grupos; aquellos que pasaban la mayor parte del día dentro de la casa (gatos domésticos) y los que permanecían fuera de ella (gatos callejeros). Se determinó que el 69% de los gatos domésticos y el 74% de los callejeros eran seropositivos. No se encontraron diferencias significativas dentro de los grupos de seropositivos para esta condición.
Estos porcentajes de seropositividad fueron mayores a los encontrados por Bergmans y col. en 1996 en Holanda, que fue de un 50% de seropositivos para gatos callejeros y de un 56% para gatos domésticos. Esta diferencia podría explicarse porque en Holanda el promedio de temperatura diaria es baja comparada con la que se tiene en Valdivia, sobre todo en los meses de verano, y por el mejor cuidado que en los países desarrollados se les brinda a los animales de compañía.
Los porcentajes de gatos seropositivos encontrados tanto en Valdivia como en Holanda indican que gatos domésticos y callejeros tienen el mismo riesgo de infectarse con B. henselae. Esto difiere de lo encontrado porChomel y col. en 1995 en California, donde un 92% de los gatos callejeros fueron seropositivos, mientras que sólo un 71,4% de los gatos domésticos dieron positivo a la reacción, lo que determinó una diferencia estadística significativa y por lo tanto un riesgo asociado a esa condición.
En el estudio realizado en la región Metropolitana por Ferres, (2000*), se encontró que la gran mayoría de los gatos muestreados eran callejeros (87%), mientras que en Coquimbo todos los gatos eran domésticos y en un tercio de ellos se consignó que salen de sus casas a tejados vecinos. Estos investigadores no encontraron diferencias significativas en la condición de seropositivos entre gatos domésticos y callejeros. El alto porcentaje de gatos seropositivos hablaría más a favor de la presentación de esta bacteria como parte de la biota del animal que de una infección.
La pulga del gato, Ctenocephalides felis, parece jugar un rol preponderante en la transmisión de B. henselae de un gato a otro y posiblemente del gato al hombre (Jameson y col., 1995; Chomel y col., 1996). Se ha demostrado que las pulgas provenientes de gatos bacterémicos tienen cultivos positivos para Bartonella henselae (Koehler y col., 1994).
Se determinó que un alto porcentaje de animales presentaba pulgas (88%) y de éstos el 75% dio positivo a la reacción. En los animales que al momento de hacer el examen clínico no se encontraron pulgas, en 4 (44%) de ellos se detectaron anticuerpos contra Bartonella henselae. Esto difiere de lo encontrado por Bergmans en Holanda en 1996, con un 53% de seropositivos en gatos sin pulgas y 41% en gatos con pulgas. El alto porcentaje de seropositivos en gatos sin pulgas puede deberse a que muchos de ellos fueron tratados con algún producto antipulgas poco tiempo antes de la toma de muestras.
De las 22 personas que fueron muestreadas, dueños de gatos positivos a B. henselae, en 4 de ellos (18%) se detectaron anticuerpos contra la bacteria. Esto concuerda con lo encontrado en Alemania por Rath y col. en 1997, que fue de 20% de seropositivos para el grupo en estudio y de 19% para el grupo control. En Suiza, Nadal y Zbinden (1995) encontraron una seroprevalencia de 12%. Al comparar los resultados de Estados Unidos en estudios diferentes realizados por Zangwill y col., (1993) y Regnery y col., (1992b), se informó de 3-4% de seroprevalencia dentro de grupos de individuos sanos, la cual es relativamente baja frente a la encontrada en Alemania, Suiza y en el presente estudio. Esto podría explicarse por el hecho de que en Estados Unidos y Suiza se tomaron muestras de sangre a grupos de individuos sanos no importando su contacto con gatos, en cambio en los estudios realizados en Alemania y en Valdivia, las muestras fueron colectadas de dueños de gato que mantenían estrecho contacto con ellos. Además hay que destacar que en este estudio los individuos muestreados eran dueños de gatos positivos a B. henselae.
*Comunicación personal: Lab. Infectología y Virología Molecular, Universidad Católica de Chile, Chile.
Aceptado: 10.01.2002.
Resumen
Con la finalidad de detectar anticuerpos contra Bartonella henselae, se obtuvo sangre de una muestra de conveniencia de 76 gatos mestizos, de ambos sexos, de 3 meses a 9 años de edad, concurrentes al Hospital Veterinario de la Universidad Austral de Chile y a otras clínicas privadas de la ciudad de Valdivia, Chile. El diagnóstico serológico se realizó mediante inmunofluorescencia indirecta. Además, se consignaron datos descriptivos sobre raza, sexo, edad, actividad y presencia de pulgas de cada uno de los gatos en estudio.
De los animales muestreados, un 71% presentó anticuerpos contra Bartonella henselae. La seroprevalencia fue de 68.4% en machos y 73.7% en hembras. Los animales con mayor porcentaje de seropositividad fueron los gatos de 3 a 6 años de edad. Veinte y nueve (69.0%) gatos que pasaban la mayor parte del tiempo dentro de la casa y 25 (73.5%) que permanecian casi todo el día fuera de la casa resultaron seropositivos. De los animales que presentaron pulgas, 50 (75.0%) tenían anticuerpos contra B. henselae.
De las 22 personas dueños de gatos positivos a Bartonella henselae, 4 (18%), evidenciaron anticuerpos contra esta bacteria.
Bibliografía
ABARCA, K. 1996. Enfermedad por arañazo de gato. Rev. Chil. Infect. 13: 78_80.
ANDERSON, B., K. SIMS, R. REGNERY, L. ROBINSON., M. J. SCHMIDT, S.GORAL, C. HAGER, K. EDWARDS. 1994. Detections of Rochalimaea henselae DNA in specimens from cat scratch disease patients by PCR. J. Clin. Microbiol. 32: 942_948.
ANDERSON, B. E., M. A. NEUMAN. 1997. Bartonella spp. as emerging human pathogens. Clinical Microbiology Reviews. 10: 203_219.
BASS, J. W., B. C. FREITAS, C. L. SISLER. 1998. Prospective randomized double blind placebo_controlled evaluation of azithromycin for treatment of cat scratch disease. Pediatr. Infect. Dis. J. 17: 447_452.
BERGMANS, A. M. C., J. W. GROOTHEDDE, J. F. P. SCHELLEKENS, J. D. A. VAN EMDEN, J. M. OSSEWAARDE, L. M. SCHOULS. 1995. Etiology of cat scratch disease: comparison of polymerase chain reaction detection of Bartonella(formely Rochalimaea) and Afipia felis DNA with serology and skin test. J. Infect. Dis. 171: 916_923.
BERGMANS, A. M. C., J. F. P. SCHELLEKNS, J. D. A. VAN EMBDEN, L. M. SCHOULS. 1996. Predominance of twoBartonella henselae variants among cat scratch disease patients in The Netherlands. J. Clin. Microbiol. 34: 254_260.
BREITSCHWERDT, E. B., D. L. KORDICK. 1995. Bartonellosis. J. Am. Vet. Med. Assoc. 206: 1928_1931.
CHILDS, J. E., J. A. ROONEY, J. L. COOPER, J. G. OLSON L. R. REGNERY. 1994. Epidemiologic observations on infection with Rochalimaea species among cats living in Baltimore. JAVMA. 11: 1775 _ 1778.
CHILDS, J. E., J. G. OLSON, A. WOLF, N. COHEN., Y. FAKILE, J. A. ROONEY, F. BACELLAR L. R. REGNERY. 1995. Prevalence of antibodies to Rochalimaea species (cat scrach disease agent) in cats. Vet. Rec. 20: 519_520.
CHOMEL, B. B., R. C. ABBOTT, R. W. KASTEN, K. A. FLOYD-HAWKINS, P. H. KASS, C. A. GLASER, N. C. PEDERSEN, J. E. KOEHLER. 1995. Bartonella henselae prevalence in domestic cats in California: Risk factors and association between bacteremia and antibody titers. J. Clin. Microbiol. 33: 2445 _ 2450.
CHOMEL, B. B; R. W. KASTEN, K. FLOYD-HAWKINS.1996. Experimental transmission of Bartonella henselae by cat flea. J. Clin. Microbiol. 34: 1952 _ 1956.
CLARRIDGE, J. E, T. J. RAICH, D. PIRWANI, B. SIMON, L. TSAI. 1995. Strategy to detect and identify Bartonellaspecies in routine clinical laboratory yields Bartonella henselae from human immunodeficiency virus positive patient and unique Bartonella strain from his cat. J. Clin. Microbiol. 33: 2107 _ 2113.
DALY, J. S., M.G. WORTHINGTON, D. J. BRENNER, C. W. MOSS, D. G. HOLLIS, R. S. WEYANT, A. G. STEIGERWALT, R. E WEAVER, M. I. DANESHVAR, C. P. O' CONNOR. 1993. Rochalimaea elizabethae sp. nov. isolated from patient with endocarditis. J. Clin. Microbiol. 31: 872_881.
HADFIELD, T. L., R. WARREN, M. KASS, E. BRUN, C. LEVY. 1993. Endocarditis caused by Rochalimaea henselae.Hum. Pathol. 24: 1140_1141.
HOLMES, A., T. GREENOUGH, G. BALADY, R. REGNERY, B. ANDERSON, J. C. O' KEANE, J. FONGER, E. Mc CRONE. 1995. Bartonella henselae endocarditis in an inmumocompetent adult. Clin. Infect. Dis. 21: 1004_1007.
JACKSON, L. A., B. A. PERKINS, J. D. WENGER. 1993. Cat scratch disease in the United States: an analysis of three national databases. Am. J. Public Health. 83: 1707_1711.
JAMESON, P., C. GREEN, R. REGNERY. 1995. Prevalence of Bartonella henselae antibodies in pet cats throughout regions of North America. J. Infect Dis. 172: 1145_1149.
KIRKPATRICK, C. E., H. E. WHITELEY. 1987. Argyrophilic, intracellular bacteria in the lymph node of a cat: cat scratch disease bacilly?. J. Infect. Dis. 156: 690_691.
KIRKPATRICK, C. E , L. T. GLICKMAN. 1989. Cat scratch disease and the role of the domestic cat: vector, reservoir and victim? Medical Hypotheses. 28: 145_149.
KOEHLER J. E., C. A. GLASER, J. W. TAPPERO. 1994. Rochalimaea henselae infection: A new zoonosis with the domestic cat as reservoir. JAMA 271: 531_535.
KORDICK, D. L., K. H. WILSON, D. J. SEXTON, T. L. HADFIELD, H. A. BERKHOFF, E. B. BREITSCHWERDT. 1995. Prolonged Bartonella bacteremia in cats associated with cat scratch disease patients. J. Clin. Microbiol. 33: 3245_3251.
LAWSON, P. A , M. D. COLLINS. 1996. Description of Bartonella clarridgeiae sp. nov. isolated from the cat of patient with Bartonella henselae septicemia. Med. Microbiol. Lett. 5: 64_73.
LUCEY, D., M. J. DOLAN, C. W. MOSS, M. GARCIA, D. G. HOLLIS, S. WENGER, G. MORGAN, R. ALMEIDA, D. LEONG, K. S. GREISEN, D. F. WELCH, L. N. SLATER. 1992. Relapsing illness due to Rochalimeae henselae in immunocompetent hosts: implication for therapy and new epidemiological associations. Clin. Infect. Dis. 14: 683_688.
MAGUIÑA, C., GOTUZZO, E. 2000. Bartonellosis. Infectious Disease Clinics of North America. 14 : 1-22.
MARGILETH, A. M. 1992. Antibiotic therapy for cat scratch disease: clinical study of therapeutic outcome in 268 patients and a review of the literature. Pediatr. Infect. Dis. J. 11: 474_478.
MAURIN, M., D. RAOULT. 1998. Bartonella infections: diagnostic and management issues. Current Opinions in Infectious Diseases 11:189-193.
NADAL, D., R. ZBINDEN. 1995. Serology to Bartonella henselae may replace tradicional diagnostic criteria for cat scratch disease. European Journal of Pediatrics 154: 906 _ 908.
NAVARRETE, M., M. S. WENZEL, R. M PINCHEIRA, L. ZAROR, M. FERRES, L. PODESTA. 1999. Espectro clínico: enfermedad por arañazo de gato. Libro resumen XXI Congreso Chileno de Microbiología "Dr.Janis Grinbergs M.". Valdivia, Chile, pp. 10-11.
RATH, P. M., G. VON RECKLINGHAUSEN, R. ANSORG. 1997. Seroprevalence of Immunoglobulin G Antibodies toBartonella henselae in Cat Owners. Eur. J. Clin. Microbiol. Infect. Dis. Lett. 16 : 326_327.
REGNERY, R. L., B. E. ANDERSON, J. E. CLARRIDGE, M. R. RODRIGUEZ-BARRADAS, D. C. JONES, J. H. CARR. 1992 a. Characterization of a novel Rochalimaea species, B. henselae sp. nov., isolated from blood of a febrile, human inmunodeficiency virus-positive patient. J. Clin. Microbiol. 30: 265_274.
REGNERY, R. L., M. MARTIN, J. OLSON .1992 b. Naturally occurring "Rochalimaea henselae" infections in domestic cat. Lancet . 340: 557_558.
SIMÓ, J., D. RIQUELME, P. ANDA. 1998. Enfermedad por arañazo de gato: Descripción de un nuevo caso. Enferm. Infecc. Microbiol. Clin. 16: 291_292.
SLATER, L. N., D. F. WECH, D. HENSEL, D. W. COODY. 1990. A newly recognized fastidious Gram_negative pathogen as a caused of fever and bacteremia. N. Engl. J. Med. 322: 1587_1593.
SPACH, D. H., K. P. CALLIS, D.S. PAAUW, Y. B. HOUZE, F. D. SCHOENKNECHT, D. F. WELCH, H. ROSEN, D. J. BRENNER. 1993. Endocarditis caused by Rochalimaea quintana in a patient infected with human inmunodeficiency virus. J. Clin. Microbiol. 31: 692_ 694.
THRUSFIELD, M. 1995. Veterinary Epidemiology, 2nd. Ed. Blackwell Science Ltda., Oxford.
UENO, H., Y. MURAMATSU, W. W. CHOMEL, T. HOHDATSU, H. KOYAMA, C. MORITA. 1995. Seroepidemiological survey of Bartonella henselae in domestic cats in Japan. Microbiol. Immunol. 39: 339-341.
VON ALLERBERGER, F., M. SCHÖNBAUER, R.L. REGNERY, M. P. DIERICH. 1995. Prävalenz von Rochalimaea henselae-Antikorpern bei Katzen in Osterreich. Wien. Tierarztl. Mschr. 82: 40_43.
ZANGWILL, K. M., D. H. HAMILTON, B. A. PERKINS. 1993. Cat scratch disease in Connecticut-epidemiology, risk factors, and evaluation of a new diagnostic test. N Engl J Med. 329: 8_13.
**El artículo fue originalmente publicado en Arch. med. vet. v.34 n.1 Valdivia 2002.