Introducción
La ganadería bovina colombiana es una actividad de gran importancia para la economía nacional. De los 51 millones de hectáreas ocupadas por el sector agropecuario, 29 millones corresponden a pastos para la utilización en ganadería, la cual genera 1.400.000 empleos directos distribuidos en 849.000 explotaciones, lo que equivale a decir que 5 millones de colombianos derivan su sustento de esta actividad. Colombia es el cuarto productor de leche de América Latina; sin embargo, el mercado lácteo en Colombia tiene un carácter restringido, debido a la falta de incentivos para la promoción de la demanda interna y la falta de apertura de nuevos mercados, ante lo cual se deben proponer políticas que impulsen el mercado.
Las exigencias del mercado hacen que el ganadero tenga que ser más competitivo y ofrecer un producto de buena calidad. De acuerdo con los organismos internacionales de referencia, la leche y sus derivados pertenecen al grupo de alimentos de mayor riesgo en salud pública no solo por tratarse de un alimento básico y de amplio consumo, sino por su susceptibilidad para transmitir enfermedades, debido a la presencia de microorganismos y contaminantes, como medicamentos veterinarios, por lo tanto, se hace necesario implementar prácticas preventivas que ayuden a disminuir las cargas patógenas y así tratar de reducir el uso de medicamentos que, además de constituirse en un factor negativo para el productor por sus costos elevados, pueden ser causa de enfermedad en el consumidor (Organización de las Naciones Unidas para la Agricultura y la Alimentación [FAO], 2006).
Aunque los residuos solo se encuentren en los alimentos en muy baja concentración, es posible que la ingestión regular de pequeñas cantidades de una misma sustancia pueda inducir a manifestaciones tóxicas a largo plazo, por efectos acumulativos (Parra et al., 2003). Así, algunas personas pueden desarrollar reacciones alérgicas por la ingestión de leche con pequeñas cantidades de antibióticos (beta lactámicos, tetraciclinas y aminoglucósidos). La principal fuente de residuos de antibióticos es la leche de vacas tratadas con estas bases vía intramamaria (Levy, 1997; Cotrino et al., 2003).
La presencia de residuos de antibióticos afecta el proceso de industrialización de la leche, pues, la mayoría de los inhibidores impiden o retardan el desarrollo de las bacterias lácticas, y ocasionan mayores costos de elaboración, de materia prima y alteración del programa de producción, que implica una pérdida de rentabilidad para la empresa (Parra et al., 2003).
El objetivo del presente trabajo fue determinar la presencia de residuos de antibiótico y establecer los tiempos de retiro en leche, en vacas tratadas con antibióticos sistémicos e intramamarios en las lecherías ubicadas en el municipio de Cartago del departamento del Valle del Cauca, así como establecer las posibles correlaciones con algunas características de producción.
Materiales y métodos
El presente estudio se llevó a cabo en tres fincas (hacienda La Miranda, hacienda Flor de Damas y finca La Lina) del municipio de Cartago, ubicado al norte del departamento del Valle del Cauca. Se encuentra en la región andina de Colombia, en una planicie a unos 917 msnm. Por la ciudad pasa muy cerca el río Cauca y, paralelo a la ciudad, el río La Vieja, que, además, sirve de frontera natural con el departamento de Risaralda. El territorio es plano y ligeramente ondulado con un área total de 279 km².
Para la población de estudio, se seleccionaron 115 vacas al azar, de cruces Holstein x cebú, con volúmenes de producción entre 6 a 22 L y un rango de edad de 2 1/2 años hasta 15 años, alimentadas bajo el sistema de pastoreo extensivo con pasturas de estrella (Cynodon nlemfuensis) y suplementación con concentrados comerciales y sales mineralizadas.
Los animales fueron tratados con antibióticos pertenecientes a diversos grupos farmacológicos. Entre los macrólidos, se utilizó espiramicina base (13.000.000 UI) y tartrato de tilosina (200 mg/mL) en posologías de 30 UI/kg/PV y 10 mg/kg/PV vía intramuscular (i.m), respectivamente. Del grupo de las tetraciclinas, se utilizó el clorhidrato de oxitetraciclina (200 mg/mL) a 10 mg/kg/PV vía i.m. Del grupo de los betalactámicos se utilizó amoxicilina trihidrato (140 mg/mL) en posología de 7 mg/kg/ PV vía i.m, una asociación de cloxacilina sódica (200 mg) y ampicilina sódica (75 mg) por inyector vía intramamaria y una cefalosporina (ceftiofur 5%) en dos presentaciones (sal sódica y clorhidrato) en posología de 2 mg/kg/PV vía i.m. En total, se usaron siete antibióticos para los diversos tratamientos de todos los animales.
El muestreo se realizó entre los meses de mayo de 2011 a abril de 2012. Las muestras de leche provenientes de diferentes cuartos fueron tomadas en tubos Vacutainer, y conservadas en refrigeración en un rango de 4-6 ºC, las cuales fueron tomadas a diferentes intervalos de tiempo (1, 3 y 12 horas) posteriores a la aplicación del antimicrobiano y luego cada 12 horas, suspendiendo el muestro en el tiempo en el cual la prueba resultara negativa a la presencia del antibiótico.
Las muestras recolectadas fueron analizadas con el kit Delvotest® SP-NT (DSM, Holanda), siguiendo las instrucciones del fabricante. Brevemente, 50 μl de leche fueron tomados y dejados a temperatura ambiente. Después, se depositaron en ampolletas que contenían Lactobacillus stearothermophilus y se colocaron en la incubadora a 64 ºC durante 3 horas. La lectura se realizó visualmente basada en cambios colorimétricos utilizando las tablas de referencia del fabricante.
Análisis estadístico
Para las variables analizadas se realizó un análisis descriptivo, exploratorio unidimensional con la determinación de media, desviación estándar y coeficientes de variación. Se utilizó un esquema [Yij = μ + τi + εi(I)], donde μ es la media, τi el efecto tratamiento y εj(i) el error experimental. Las variables de respuesta fueron tiempo de persistencia del antibiótico en la leche, expresado en horas. Se crearon rangos de volumen de producción, días en leche y tiempo de persistencia antibiótica. Los datos fueron analizados mediantes tablas de contingencia, prueba de x2 de independencia, que permitieron inferir el efecto tratamiento sobre la respuesta de persistencia del antibiótico; esto cotejando el valor de la tabla de x2, incluso el análisis de los grados de libertad (gl). Además, se establecieron correlaciones estadísticas mediante determinación del coeficiente Rho de Spearman, siguiendo lo descrito por Restrepo y Gonzales (2007), y posterior a la validación de los supuestos estadísticos. Los datos fueron analizados mediante el uso del software SPSS® versión 20 para Windows (IBM, EE. UU.).
Resultados y discusión
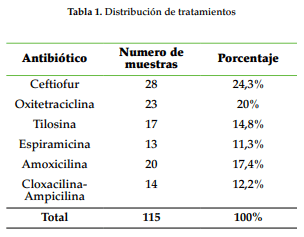
Un total de 115 muestras fueron recolectadas y distribuidas en seis tratamientos con siete antimicrobianos, como se muestra en la tabla 1. Esta distribución de tratamientos se debe a la facilidad de medicamentos que los ganaderos proporcionaron para el trabajo de investigación.
Análisis de residualidad de antibióticos
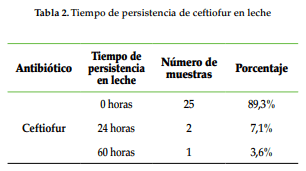
Un estudio realizado por Báez et al. (2009) evaluó la residualidad en leche de una suspensión inyectable a base de ceftiofur sódico (50 mg/ml) en seis vacas de producción de leche, provenientes de tres fincas de la Sierra (Ecuador) y analizadas con la prueba microbiológica Copan Milk Test (StandAlone Company, Italia), y se obtuvieron resultados que indicaron que el compuesto activo no tiene residualidad en leche. Otro estudio realizado en 30 muestras de leche a tres concentraciones de ceftiofur evaluó la sensibilidad de las pruebas microbiológicas para la detección del antimicrobiano en la leche, tanto para la prueba Copan Milk Test (Stand-Alone Company, Italia) como para el Delvotest SP-NT (DSM, Holanda), que demostró que el límite de detección del antibiótico en leche, para las dos pruebas, debe ser igual o superior a los 100 μg/l (Borrás, 2011), en comparación con un estudio realizado por la Organización de las Naciones Unidas para la Agricultura y la Alimentación (FAO), en asocio con la Organización Mundial de la Salud (OMS), en el cual recuperaron, mediante cromatografía líquida de alta precisión (HPLC), 50 μg/l de desfuroilceftiofur (residuo con actividad antimicrobiana) en leche que no superaron el límite máximo de residualidad (LMR) permitido para este antibiótico, el cual es de 100 μg/L (FAO/OMS, 1996). Para el presente estudio, se trataron 28 vacas con ceftiofur, de las cuales el 89,3% fueron negativas a trazas del antibiótico (Tabla 2). Según los resultados obtenidos por otros autores y comparados con los del presente estudio, se puede inferir que la prueba microbiológica tiene escasa sensibilidad para detectar trazas del antibiótico, sin embargo, el medicamento no tiene tiempo de retiro porque no supera los LMR establecidos por el Comité. Para el 10,7% restante de vacas tratadas con ceftiofur, se utilizó un producto comercial de combinación con meloxicam, un antiinflamatorio no esteroidal (AINE), el cual dio una persistencia en leche de 24 a 60 horas; los resultados obtenidos pueden ser atribuibles a la capacidad de diferente unión a proteínas plasmáticas de los dos compuestos utilizados, que, en este caso, es del 99% para los AINE (Bueno, 2009) y del 92% para el ceftiofur (Manual de laboratorio farmacología veterinaria, 2011), por lo tanto, el compuesto de mayor afinidad a proteínas plasmáticas desplaza al de menor afinidad, y aumenta la fracción libre de este último (Botana et al., 2002). La fracción libre incrementa la cantidad de fármaco para difundir libremente a través de los tejidos (Anadón et al, 2011) con mayor distribución del antimicrobiano en la glándula mamaria (Boggio y Litterio, 2010); por consiguiente, para este caso, se puede inferir que aumentaría la concentración del antimicrobiano en la leche, haciendo detectable el fármaco por la prueba microbiológica (kit Delvotest SP-NT).
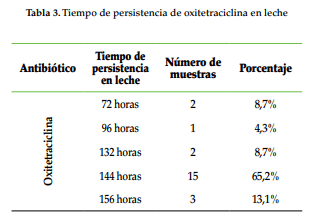
Otro estudio realizado en 138 vacas tratadas con una variedad de productos antibióticos en granjas lecheras del suroeste de Ontario (Canadá), dentro de las cuales se trataron 17 vacas con oxitetraciclina, reportó que la persistencia del antimicrobiano no supera las 72 horas (McEwen et al., 1992). Para esta investigación, un 8,7% de los resultados concuerda con los obtenidos por los investigadores antes nombrados; el 91,3% restante oscila entre 96 y 156 horas de persistencia (Tabla 3), coincidiendo con los resultados obtenidos por San Martín et al. (1995). Por su parte, la variabilidad individual observada en relación con los tiempos de retiro puede ser atribuida, principalmente, a las diferencias fisiológicas entre los individuos, tal como ha sido mencionado por San Martín et al. (1995). Otro aspecto para tener en cuenta, en la diferencia de los resultados obtenidos y los observados en el trabajo de McEwen, es la cantidad de ordeños por día que pueden manejar en lecherías especializadas, los cuales son superiores a los realizados en lecherías tropicales, por lo tanto, la tasa de excreción del antibiótico en la leche puede ser más alta en este último caso.
Otro aparte del estudio incluye el tratamiento de 17 vacas con tilosina (Tabla 4), de las cuales el 94,1% marcó un tiempo de persistencia entre 108- 120 horas que son comparables a los resultados obtenidos por Rico y Ferraro (2010), en un grupo de cinco vacas, después de la inyección intramuscular de 17,6 mg diarios de tilosina por kilogramo de peso. Durante cinco días los residuos en la leche persistieron en un rango de tiempo de 108-144 horas, detectados por un método microbiológico en el que se empleó Sarcina lutea como microorganismo de experimentación. El 5,9% de animales del estudio actual tuvo una persistencia de tilosina en la leche de 168 horas, lo cual puede ser atribuible a un manejo inadecuado de las muestras que hayan tenido contacto con desinfectantes o a procesos patológicos que modifican la permeabilidad de la glándula mamaria y que hacen que el medicamento se elimine lentamente.

Las muestras de leche de seis vacas tratadas con espiramicina y analizadas mediante HPLC determinaron una concentración de 1 mg/L después de ocho ordeños (cuatro días) y 0,09 mg/L a los 17 ordeños (8,5 días) (OMS, 1991). Datos similares obtuvieron Renard et al. (1994), con tiempos de 85 – 105 horas de persistencia del antibiótico en leche. Para el presente estudio, el 69,2% de los resultados obtenidos (Tabla 5) coincide con los observados en el trabajo de Renard et al. (1994), y el porcentaje restante está dentro del rango de tiempo de persistencia mostrado en el trabajo realizado por la OMS (Levy, 1997).

Cerutti et al. (2002) analizaron, mediante una prueba microbiológica (Charm® AIM-96), muestras de leche de seis vacas medicadas con amoxicilina, y determinaron un tiempo de persistencia del antibiótico en leche de 84 horas en siete ordeños, que concuerda con el 65% de los resultados obtenidos en el presente trabajo de investigación (Tabla 6). El 35% restante de los resultados marcaron una persistencia entre 48 y 72 horas, coincidiendo con los resultados obtenidos por San Martín et al. (1995).

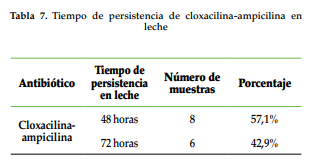
Referente a tratamientos intramamarios, Booth (citado por Ocampo y Sumano, 2006), en 1986, realizó un estudio con antimicrobianos comerciales de diferentes bases farmacológicas, y encontró que, para la combinación cloxacilina-ampicilina, el tiempo de persistencia fue de 60 horas, sin variación a lo estipulado para el producto comercial; en contraste al estudio actual, se encontró que el 42,9% de los resultados obtenidos concuerdan con los observados en la investigación antes nombrada, pero no se encontró variación en el tiempo de retiro especificado por las casas comerciales de estos productos. El 57,1% restante de los resultados obtenidos en la investigación marcó una persistencia del antibiótico por 48 horas (Tabla 7), compatible con los tiempos de retiro especificados por Ocampo y Sumano (2006). Aunque hubo una pequeña variación de los resultados obtenidos en el estudio, se puede pensar que las diferencias en las formulaciones de varias casas farmacéuticas influyen sobre la tasa de eliminación del medicamento. En este sentido, San Martín et al. (1998) reportan que los excipientes en que se vehiculiza el antibiótico inciden en la liberación y eliminación de un fármaco. Otro aspecto por tener en cuenta es el tamaño de partícula del principio activo, como lo reporta Ehinger y Kietzmann (1998): que las formas micronizadas (<10 μm) alcanzan mayores concentraciones en el tejido mamario en comparación a las partículas grandes (>40 μm); en este caso, se puede inferir que, al haber mayor unión del fármaco a proteínas tisulares, la fracción libre disminuye en la leche y, por ende, el tiempo de eliminación será menor.
Un factor importante que puede modificar los resultados de las pruebas microbiológicas es la presencia de inhibidores naturales en la leche, como la enzima lactoperoxidasa (LP), que, bajo la influencia de otros componentes, como el peróxido de hidrogeno (H2 O2) y el tiocianato (SCN), dependiendo del tipo de alimentación, activan la enzima lactoperoxidasa, que ejerce una acción inhibidora sobre una gran variedad de microorganismos grampositivos y gramnegativos (Althaus et al., 1998). Referente a esto, se puede inferir que la acción de dicho sistema puede producir inhibición de los microorganismos del kit Delvotest SP-NT utilizado para el análisis de la investigación presente.
Althaus et al. (1998) observaron que las enzimas LP y H2 O2 disminuyen su concentración a medida que avanza los días de lactación, por lo tanto, la concentración de estas enzimas resultan insuficientes para activar el sistema. Los autores sugieren la necesidad de realizar investigaciones sobre la influencia de las pruebas microbiológicas en la determinación de residuos de antibióticos y su correlación con la alimentación y tiempo de lactancia del animal.
Análisis de correlación
Los resultados de correlación obtenidos en el presente estudio muestran que la relación que existe entre el tipo de antibiótico y tiempo de persistencia (X2 = 220,666; gl = 15; p = 0,000) supera, en gran medida, los recuentos esperados (X2 = 7,26), y, como la significancia es menor de 0,05, se rechaza la hipótesis nula, lo que indica que existe un grado de relación alto entre estas dos variables.
En la relación de volumen de producción frente a tiempo de persistencia, se encontró un valor (X2 = 0,813; gl = 3; p = 0,846) que supera al valor crítico esperado (X2 = 0,35); sin embargo, la significación es mayor de 0,05, por lo tanto, se acepta que el volumen de producción no influye sobre el tiempo de persistencia del antibiótico.
Para las variables días en leche frente a tiempo de persistencia, con (X2 =17,486; gl = 15; p = 0,291), es mayor del valor crítico esperado (X2 = 7,26) y de la significación 0,05, por lo tanto, se acepta que los días en leche no tienen correlación sobre el tiempo de persistencia del antibiótico.
En relación con las variables edad del animal y tiempo de persistencia del antibiótico, los resultados (X2 = 10,612; gl = 3; p = 0,014) son mayores del valor esperado (X2 = 0,35); sin embargo, como el valor de significación es menor de 0,05, se rechaza Ho y, por lo tanto, existe una influencia de la edad del animal sobre el tiempo de persistencia del antibiótico.
Asimismo, el análisis de correlación Rho de Spearman arrojó solo significancia de correlación para antibiótico frente a tiempo de persistencia (0,402; p = 0,00), días en leche frente a tiempo de persistencia (0,232; p = 0,014) y edad frente a tipo de antibiótico (0,258; p = 0,006).
Control de residuos en Colombia
En Colombia, no se cuenta aún con datos precisos y legales de los niveles de tolerancia para cada medicamento utilizado en bovinos productores de leche, por lo que se recurre, con frecuencia, a los datos contenidos en el Codex alimentarius. Desde 1998 Colombia, mediante el Decreto 977 de 1998, crea oficialmente el Comité Nacional del Codex Alimentarius para formular políticas relacionadas con los procesos adelantados en la Comisión Mixta FAO/OMS de este organismo (Ministerio de Salud, 1998), en la que se incluye la regulación de residuos de medicamentos en productos animales.
De igual forma, para contribuir con la calidad de los productos de origen bovino, en el 2004 se crea por Ley de la República el Sistema Nacional de Identificación e Información de Ganado Bovino (SINIGAN); esta iniciativa pretende de manera gradual lograr la identificación total del hato nacional y reconocer la procedencia de un bovino o de sus productos apoyando así la salud pública nacional (Congreso de la República de Colombia, 2004).
La entrada de productos importados que compiten con los locales en calidad, trazabilidad y precio, obliga a los ganaderos a mejorar la calidad e inocuidad con el objeto de mantener y mejorar su posición dentro del mercado interno, por lo cual se introduce un sistema de acciones con el propósito de orientar al productor primario en buenas prácticas ganaderas para la producción de leche, las cuales están reglamentadas por el Decreto 616 de 2006, expedido por el Ministerio de la Protección Social, el Ministerio de Agricultura y Desarrollo Rural, y por la Resolución 3585 de 2008, del Instituto Colombiano Agropecuario (ICA).
En Colombia han sido varios los estudios que se han desarrollado con respecto a la residualidad de fármacos en alimentos de origen animal; sin embargo, muchos de estos no han sido divulgados masivamente a través de comunicaciones científicas, lo que impide vislumbrar claramente el avance real del país en esta materia (Lozano y Arias, 2008).
Los antimicrobianos representan una gran proporción de medicamentos utilizados en animales destinados al consumo o sus derivados, siendo los grupos más destacados los β-lactámicos (penicilinas sintéticas y cefalosporinas), tetraciclinas (oxitetraciclina), macrólidos (espiramicina y tilosina), entre otros (Boggio y Litterio, 2010), y, aunque las casas farmacéuticas, dentro de sus recomendaciones de uso de estos medicamentos, incluyen tiempo de retiro, los estados metabólicos, edad, volumen de producción del animal, entre otros, influyen en la tasa de eliminación del medicamento y, por ende, la residualidad de este se verá modificada. Con este estudio, se buscó establecer los tiempos de retiro dependientes de los factores antes mencionados, procurando ofrecer un producto inocuo para el consumo humano y que, además, mitigue el impacto de este en la economía del productor.
Conclusiones
Colombia carece de información sólida sobre el estatus sanitario de residuos en alimentos de origen animal, así como de sistemas de diagnóstico, que permitan cuantificar esta problemática, por lo tanto, se requiere incrementar la cantidad de trabajos referentes a la residualidad, con el fin de evaluar si las recomendaciones de los laboratorios farmacéuticos son adecuadas y así contribuir a la misión de la protección de la salud pública.
Los resultados del presente artículo permiten inferir que los tiempos de retiro de los antibióticos deben ser reevaluados con el fin de dar una mayor certeza en campo de los residuos de estos fármacos en productos de consumo humano, específicamente la leche.
La oxitetraciclina fue el antibiótico que demostró mayor duración en la leche sin excluir la alta persistencia de antibióticos pertenecientes a otros grupos funcionales.