Introducción
En México, la raza Simmental se introdujo en 1973, procedente de Alemania y Suiza. Estos animales tienen buena adaptación en climas árido, semiárido y trópico húmedo (1), no obstante, el estrés calórico provoca mayor consumo de oxígeno y conduce a hipoxia celular (2).
A nivel molecular, el estrés calórico induce la expresión de la familia de genes de proteínas de choque térmico (HSP). Las proteínas HSP’s se clasifican en 6 familias, de acuerdo a su peso molecular, las cuales son HSP110/105, HSP90, HSP70, HSP60, HSP40 y sHSP. De manera particular, HSP60 está implicada en la reactivación de las proteínas desnaturalizadas, en el impedimento de la formación de agregados termodinámicamente inestables y en la comunicación intercelular de la respuesta inmune, mientras, HSP90 participa en la inmunidad innata, reorganización de la cromatina y modificaciones epigenéticas (3).
Dentro de los 30 cromosomas que contiene el genoma bovino, el gen HSP60 se encuentra en el cromosoma 2, mide 30.39 kb, tiene 11 exones y 10 intrones y su mRNA mide 10,396 nt. El gen HSP90 se encuentra en el cromosoma 23, mide 25.63 kb, tiene 11 exones y 10 intrones y su mRNA mide 5,662 nt. El gen constitutivo β actina se encuentra en el cromosoma 25, mide 23.41 kb, tiene 5 exones y 4 intrones y su mRNA mide 3,414 nt (4).
A través de la técnica de qPCR, se pueden generar millones de copias de fragmentos de mRNA’s de genes particulares con alta especificidad y sensibilidad, con fines de análisis de expresión, entre otras aplicaciones (5).
El éxito del método qPCR depende de varios factores como la temperatura de alineamiento de los iniciadores y de la sonda marcada con fluorescencia, las concentraciones de los reactivos, la concentración y calidad de los ácidos nucleicos, entre otros. Durante el establecimiento e implementación de un diseño qPCR, las condiciones experimentales deben ajustarse para la obtención de los fragmentos amplificados de interés (5).
Objetivo.
Optimizar las condiciones de amplificación de los genes HSP60, HSP90 y β-actina en cDNA bovino para análisis de expresión relacionado con estrés calórico.
Material y métodos
Se incluyeron 10 muestras de sangre total con EDTA de bovinos de la raza Simmental procedentes de un rancho de la localidad de Puerto Vallarta, Jalisco. La extracción y purificación de mRNA total se llevó a cabo con el método comercial SV Total RNA Isolation System de la marca Promega. El mRNA obtenido se cuantificó y se verificó la pureza por espectrofotometría en un equipo NanoDropTM 2000 de la marca Thermo Fisher ScientificTM. En la determinación de la concentración de mRNA se consideró el valor de 40 como coeficiente de extinción. La síntesis del cDNA se realizó por retrotranscripción del mRNA aislado con el método comercial GoScriptTM ReverseTranscription System de la marca Promega. El cDNA obtenido se cuantificó y se verificó la pureza por espectrofotometría en un equipo NanoDropTM 2000 de la marca Thermo Fisher ScientificTM. En la determinación de la concentración de mRNA se consideró el valor de 33 como coeficiente de extinción. Las muestras de cDNA se estandarizaron a 500 ng/μL de concentración con agua libre de nucleasas estéril. Después, se realizó una solución de trabajo de las muestras a 100 ng/μL. Los genes HSP60, HSP90 y β-actina se amplificaron con iniciadores sentido, antisentido y sondas marcadas con fluorescencia diseñados por una compañía comercial. Las secuencias de iniciadores y sondas son omitidas por cuestión de propiedad intelectual. El tamaño esperado de los fragmentos fue de 159 pb en HSP60, 102 pb en HSP90 y 94 pb en β-actina. La amplificación se llevó a cabo por qPCR dúplex del gen HSP60 o HSP90 y β-actina. La mezcla de reacción se realizó en un volumen final de 15 μL, con 1X de TaqMan® Fast Advanced Master Mix de la marca Thermo Fisher ScientificTM, 300 nM de los iniciadores sentido y antisentido de cada gen, 180 nM de sonda de los dos genes, 200 ng de DNA y el volumen se completó con agua libre de nucleasas estéril. Las condiciones de amplificación fueron un ciclo de desnaturalización inicial a 95°C por 10 minutos y 45 ciclos de desnaturalización a 95°C por 15 segundos y alineamiento/extensión a 65°C por 60 segundos. El termociclado se llevó a cabo en un equipo StepOnePlusTM Real-Time System. Los resultados se analizaron con el programa StepOnePlusTM Software v2.1.
Resultados
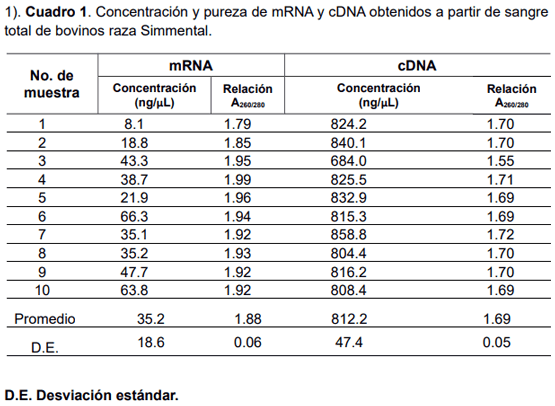
En la cuantificación de RNA mensajero total se obtuvieron valores de 8.1 a 66.3 ng/μL y con respecto a la pureza, en la relación A260/280 se observaron valores de 1.79 a 1.99 (cuadro 1). Por otra parte, los valores de concentración de cDNA fueron de 684.0 a 858.8 ng/μL y los valores de la relación A260/280 fueron de 1.55 a 1.72.
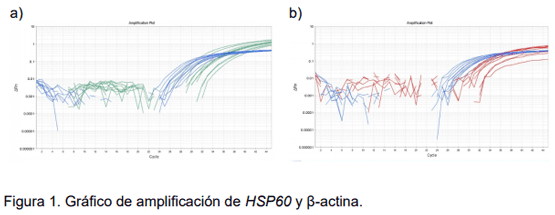
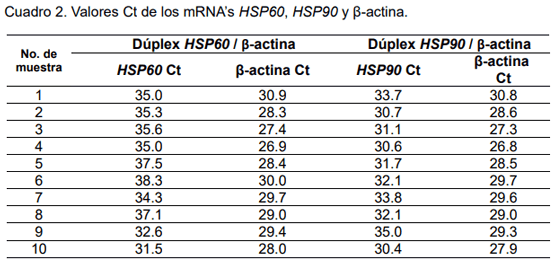
En el análisis de la gráfica de resultados de la amplificación por qPCR dúplex de HSP60 (verde) y β-actina (azul), se observa la curva típica de amplificación en ambos mRNA’s (figura 1 a). Los valores Ct del mRNA HSP60 fueron de 31.5 a 38.3, y del mRNA β-actina fueron de 26.9 a 30.9 (cuadro 2).
Por otra parte, en la figura 1 b se observa, la curva típica de amplificación de los mRNA’s HSP90 (rojo) y β-actina (azul). Los valores Ct del mRNA HSP90 fueron de a 35.0 y del mRNA β-actina fueron de 26.8 a 30.8 (cuadro 2).
Discusión
Durante la extracción de mRNA total se observó un amplio rango de concentraciones, además, la muestra 1 presentó baja cantidad (8.0 ng/μL) no obstante, a través de la transcripción inversa se obtuvieron cantidades similares de cDNA, a excepción de la muestra 3 (684.0 ng/μL).
La curva típica de amplificación contiene las fases inicial, exponencial y plateau. No se considera la obtención de amplificado en los gráficos que no presentan estas características. En los resultados obtenidos durante la amplificación qPCR dúplex HSP60 y β-actina y qPCR dúplex HSP90 y β-actina, se observa el gráfico con la curva típica, de tal manera que se obtuvo amplificación de los dos genes en ambos ensayos.
El valor Ct es el ciclo en el cual comienza la fase exponencial y es inversamente proporcional a la cantidad de copias del gen de interés. En las muestras analizadas, los valores Ct de los tres blancos se observaron de 26.8 a 38.3, lo cual está dentro de lo esperado, puesto que, Ct con valores menores a 20 y mayores a 38 no se considera amplificación. Además, los valores de Ct de β-actina son menores a los valores Ct de los mRNA's HSP60 y HSP90, de acuerdo con lo esperado por ser un gen constitutivo.
La amplificación de los mRNA’s HSP60 y HSP90 en relación con el mRNA β-actina constitutivo permitirá conocer el nivel de expresión en bovinos bajo condiciones de estrés calórico. Estos genes fueron seleccionados por la relación con niveles de expresión elevados durante estrés calórico, reportado en la literatura (6), no obstante, tales estudios fueron realizados a nivel de proteína y no se ha realizado, hasta nuestro conocimiento, a nivel mRNA.
Conclusiones
Las condiciones de amplificación de los genes HSP60, HSP90 y β-actina en cDNA bovino para análisis de expresión relacionado con estrés calórico se optimizaron.





.jpg&w=3840&q=75)