Bio-transferencia de aflatoxina B1 a aflatoxina M1, del alimento a la pechuga de gallinas ponedoras.
La presencia de metabolitos hidroxilados de la aflatoxina B1 (AFB1), tales como la aflatoxina M1 (AFM1) han sido reportados en pechuga de gallina ponedora, Díaz Zaragoza et al, 2014. Las gallinas cuando terminan su ciclo de postura son enviadas al rastro para su sacrificio.
En México el consumo de gallina, en forma de caldo, tiene mucha demanda principalmente en el centro y sureste del país. Algunas empresas procesan la carne de gallina para preparar diversos tipos de embutidos, de tal manera que de una u otra forma se transforma en un alimento para consumo humano. Actualmente el Sistema Producto Aves está trabajando para hacer conciencia sobre la inocuidad de los alimentos generados en la industria avícola como el huevo y la carne. La AFM1 es un compuesto considerado como cancerígeno y se limita en leche a niveles de 0.5 a 0.05 µg/L, dependiendo de la normatividad de cada región del mundo. Ante la posibilidad de que la AFM1 sea un riesgo químico en el consumo de pechuga de gallina. Se realizó la evaluación de la Bio-transferencia de la AFB1 presente en una dieta contaminada con 500 µg/kg (ppb) y cuantificar la contaminación con AFM1 en la pechuga, después de 8 días de consumo. Al mismo tiempo se incluyó un agente anti-aflatoxinas para verificar su eficiencia en este experimento.
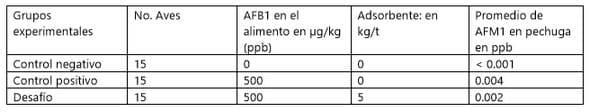
La concentración de AFM1 en la pechuga del grupo control negativo fue menor al límite de detección de 0.001 ppb. En las pechugas del control positivo la concentración fue de 0.004 ppb y en el grupo de desafío la concentración fue de 0.002 ppb. Los ensayos analíticos se efectuaron por la técnica de cromatografía de líquidos de ultra resolución (UPLC).
Los resultados obtenidos demuestran que la biotransferencia de la AFB1 a la pechuga como AFM1 es mínima. Por lo tanto este alimento se considera como inocuo. La eficiencia del adsorbente evaluado fue del 50 %. De manera complementaria se evaluó la concentración de la AFB1 en el hígado, donde se cuantifico esta toxina a niveles de 0.5 ppb en el grupo control positivo y 0.2 ppb en el grupo de desafío con adsorbente. Siendo del 60 % la efectividad del adsorbente comercial.
Palabras clave: Inocuidad pechuga, aflatoxinas B1 y M1, adsorbentes micotoxinas.
La generación de alimentos inocuos de origen animal en México, destinados al consumo humano ha tomado una relevancia muy importante a partir del año 2014 en que el Sistema producto ave ha enfocado su atención en verificar la presencia de sustancias indeseables en los alimentos para aves, destinadas a la producción de carne y huevo. Se ha considerado que las gallinas ponedoras una vez que cumplen su ciclo de producción y se destinan al consumo humano pueden contener aflatoxina B1 o sus derivados hidroxilados, como la AFM1, en la pechuga. Esto ha sido reportado en México, Díaz Zaragoza et al. 2014. Ante la posibilidad que las AFM1 sea un riesgo de inocuidad, para los consumidores de gallina vieja, se realizó un experimento para verificar la bio-transformación de AFB1 a AFM1 del alimento contaminado a la pechuga.
- M. Diaz-Zaragoza, *M. Carvajal-Moreno, I. Mendez-Ramirez, N.C. Chilpa-Galvan, E. AvilaGonzalez and C.M. Flores-Ortiz. Aflatoxins, hydroxylated metabolites, and aflatoxicol from breast muscle of laying hens. 2014. Poultry Science 93:3152-3162.
- Manual de Buenas Practicas Pecuarias Producción de huevo para Plato. SENASICA, SAGARPA, Gobierno Federal. México 2010.
Estimados autores, considero que este artículo tiene un importante aporte en la seguridad agroalimentaria y salud publica veterinaria, ensayos como este contribuyen a dar algunas respuestas o a veces más dudas científicas razonables, que ayudan a las soluciones y tomar de decisiones sobre el problema de las micotoxinas en alimentos de origen animal, destinados al consumo humano.
Tengo algunas reflexiones que quisiera compartir. Recordemos que a partir de la molécula de AFB1, se puede derivar por biotransformación principalmente hepática, no solo AFM1, también puede originarse otros metabolitos, tales como, conjugados de AFB1 los cuales tienen mayor polaridad al agua y más peso molecular, siendo entonces menos tóxicos y fácilmente excretados en orina o bilis. Otros más tóxicos como el AflatoxinaB1-8,9-Epóxido (AFB1- Epóxido) y reservorios o de toxicidad latente como Aflatoxicol entre otros.
El Aflatoxicol es relativamente de escasa o ninguna citotoxicidad en varias especies animales, pero puede eventualmente biotransformarse en AFB1 nuevamente y retomar rutas de biotransformación (por enzimas de Fase 1 de la superfamilia CYP450 primordialmente) convirtiéndose por ejemplo en AFM1, la cual es aproximadamente 9 veces menos carcinogénica que la AFB1 para el humano, basado en un consumo expresado en microgramos/Kg de peso corporal (pc)/día. También pueden resultar otros metabolitos derivados de AFB1 más tóxicos como AFB1-Epóxido, el cual es considerado altamente hepatotóxico, mutagénico y hepatocarcinogénico en humanos y otras especies, siendo las gallinas menos susceptibles al mismo.
Una vez ingerida una dieta contaminada con niveles determinados, estos metabolitos derivados de AFB1 podrían aparecer en estas aves en mayor o menor concentración, según la ruta metabólica que se promueva primordialmente en el hepatocito, por su mayor expresión génica de CYP450, en comparación con otros tejidos, tales como, el musculo esquelético cuya expresión y cantidad de CYP450 es considerablemente menor a la del hígado.
La capacidad de metabolismo hepático del AFB1- Epóxido en Gallus gallus domesticus y sus líneas genéticas, son muy eficiente debido a la alta expresión de epóxidos-hidrolasas hepáticas, que pueden disminuir la toxicidad de este derivado de AFB1.
Por eso estoy en acuerdo con los autores del presente artículo, en no coincidir con lo que describe el “Manual de Buenas Prácticas Pecuarias producción de huevo para plato, en La pagina 51, de la edición 2010, especifica: Sólo una cosa es cierta, los animales no son capaces de descomponer las micotoxinas y las transmiten directamente a los seres humanos mediante la cadena alimentaria.….”. En razón de que las líneas genéticas de Gallinas ponedoras, posee un sistema hepatobiliar con atributos de especie que metabolizan y eliminan eficientemente AFB1 y derivados en un estado de salud normal.
En este orden de ideas, según algunos autores*, en humanos la ingesta de micotoxina diaria que puede ser tolerada (TDI) para AFB1 es entre 0,11 y 0,19 ng/Kg/pc/día, con un nivel de riesgo de 1/100000. Describiéndose un valor estimado de TDI para la AFM1 de 2ng/Kg/pc/día, lo que representa aproximadamente diez veces más nivel de tolerancia que la AFB1, comparado con el mayor valor de TDI para la AFB1.
*Fuente:
-Gimeno 2007. En: Residuos de Aflatoxinas y Ocratoxina A en Alimentos de Origen Animal Residuos de Aflatoxinas y Ocratoxina A en Alimentos de Origen Animal (Leche, Huevos, y Tejidos Comestibles). Publicado el: 12/06/2007, en este portal web.
-Kuiper-Goodman, T., 1994. “Prevention of Human Mycotoxicoses Trough Risk Assesment and Risk Management”. In: J.D.Miller and H.L.Trenholm (eds.), Mycotoxins In Grain, Compouns Other Than Aflatoxin. Eagan Press, St.Paul, Minnesota, pp. 439-469.
Sin embargo, Estos parámetros e indicadores son estimados para humanos adultos promedio con normal estado de salud. Asimismo, la concentración o presencia en hígado y musculo esquelético de residuos AFM1 y otros metabolitos tóxicos o no tóxicos dependerá primordialmente del funcionamiento hepatobiliar y renal del ave para biotrasnformar y excretar, y no exclusivamente de la cantidad de aflatoxina en la dieta contaminada y la frecuencia de ingestión de la misma por las aves. Siendo este funcionamiento fisiológico dependiente de ciertas variables intervinientes: los antecedentes de estrés, alimentación/nutrición, bioseguridad, desafíos infectocontagiosos de la parvada, manejo, exposición a climas extremos, fármacos, aditivos y otros tóxicos (plaguicidas clorados o fosforados, metales pesados, otras micotoxinas, etc).
Estos aspectos presentes (frecuentes o eventualmente) en la avicultura comercial, (pero ausentes o controlados con aves expuestas a dietas experimentales contaminadas con aflatoxinas), pueden inducir resultados muy distintos a los obtenidos en niveles de residuos de AFB1 y otros de sus metabolitos en tejidos, cuando se hace investigaciones monitoreadas. Lo cual se debe considerarse al concluir y discutir este tipo de ensayos controlados.
Adicionalmente, el hígado humano en comparación con aves de postura, tiene menos expresión de epóxido-hidrolasas y eficiencia para metabolizar el AFB1- Epóxido, siendo esta una entre varias razones por la que las aflatoxinas son el principal hepatocarcinogénico en humanos, debido a la afinidad por ácidos nucleícos celulares y propiedad mutagénica del mencionado epóxido.
Considerando al humano el último eslabón de la cadena agroalimentaria, hay que tomar en cuenta ciertos aspectos de nuestra especie que nos pueden hacer menos o más susceptibles a las aflatoxinas del punto de vista toxicocinético y toxicodinámico, debiendo recordar la triada epidemiológica o ecológica para el riesgo de cualquier exposición tóxica (Toxina-Hombre-Ambiente) a la cual no escapan las aflatoxinas.
Suponiendo que gallinas ponedoras a nivel de campo se exponen a dietas contaminadas con determinados valores de aflatoxinas, su tejido hepáticol, musculo esquelético y productos derivados por ejemplo, podrían contener una concentración baja de residuos AFB1 o sus metabolitos derivados de escasa o alta toxicidad, dependiendo esto primordialmente de su buen funcionamiento hepatobiliar/renal (afectado eventualmente por otras tóxicos, estrés/desafíos ambientales y de manejo ya mencionados), y no solo de los niveles de aflatoxinas ingeridas en la dieta y tiempo de exposición a la misma.
Pero el razonamiento para el riesgo de si esos bajos niveles de residuos de AFB1 en tejidos de aves, son “inocuos” o no para el humano, involucra también considerar la continuidad o frecuencia de ingesta del alimento con residuos y a que consumidor humano va dirigido ese alimento o producto procedente de las gallinas ponedoras (micotoxina-hombre-ambiente).
La “inocuidad” o riesgo de toxicidad no será igual si el consumidor es un infante, mujeres embarazadas, pacientes con enfermedades o alteraciones hepáticas/renales crónicas, o personas simplemente cuyos ambientes laborales o domésticos permitan exposición a otros tóxicos o xenobíticos, que interaccionen toxicocinéticamente en biotransformación/eliminación y puedan bloquear o estimular rutas metabólicas o de excreción de esos niveles de residuos de metabolitos de AFB1, a un ritmo distinto al esperado en un adulto sano.
Es por ello que debo decir, respetando la opinión de los autores, que no comparto el término “inocuo” cuando se trata de bajos niveles de residuos de AFB1 y sus metabolitos en tejidos musculo esquelético de gallinas destinados a consumo humano. En este caso la inocuidad es muy relativa y dependiente de variables intervinientes en el ambiente del ave y del consumidor final (Micotoxina-Ave-AMBIENTE/AMBIENTE-Hombre-Micotoxina).
Considero que bajos niveles de aflatoxinas y de sus metabolitos en tejidos o huevos, no son necesariamente seguros o inocuos (según Micotoxina-Hombre-Ambiente), simplemente serán menos nocivos y deberían considerarse como marcadores e indicadores a nivel de campo o experimentales, para evaluar la eficiencia metabólica de estas aves con y sin condiciones de desafíos ambientales, contra estas micotoxinas y tomar decisiones en control de calidad y trazabilidad del proceso productivo.
En razón de que personas por ejemplo, expuestas a ambientes laborales o domésticos con humo forestal/urbano o de hábitos fumadores (activos y pasivos), residuos de plaguicidas fosforados o clorados, promoverán que su hígado exprese mayores isoenzimas de la familia CYP450 (inducción enzimática), pudiendo incrementar la frecuencia de biotrasformación de AFB1 al AFB1- Epóxido, metabolito de mayor toxicidad y oncogenicidad. Igualmente, la inmadurez hepática y renal infantil o fetal, podría hacer menos eficiente la biotransformación y eliminación de metabolitos de AFB1 en comparación con un adulto sano. Aquellos pacientes con compromiso hepatobiliar o renal podrían biotransformar y excretar con dificultad los residuos de AFB1 y sus metabolitos (AFM1, aflatoxicol, entre otros) en relación a una persona sana. Por lo que los factores de riesgo se deben considerar por la complejidad que estos agregarían a esta problemática agroalimentaria.
Lo anteriormente expuesto, no es con el fin de crear rechazo al consumo de pechuga de gallina y en alimentos derivados de la industria avícola o infundir miedos ilógicos a los comensales de agroproductos de origen animal. Simplemente, lo que pretendo es reflexionar sobre el uso o empleo del término “inocuidad”… en la interpretación y necesaria discusión de los importantes resultados de relevantes ensayos controlados, tales como, los que se presentan en este foro que reportan niveles de residuos de aflatoxinas en tejidos comestibles de aves expuestas a dietas contaminadas en ensayos controlados.
Mis disculpas por lo extenso del comentario…
Mis respectos a los autores por la relevancia y gran aporte de sus experimentos.








