Introducción
La Enfermedad de Newcastle (EN) es sin duda alguna una de las mayores preocupaciones de la industria avícola en México debido a las grandes pérdidas económicas que causa cuando se presenta de manera clínica o subclínica (8). El vEN fue reportado por primera vez en México en 1946 (10), aunque es muy probable fuera introducido al país mucho tiempo atrás, sin embargo, como la avicultura en esa época consistía en pequeños gallineros, las pérdidas nunca se consideraron de gran magnitud. A partir de los años 50’s, la avicultura mexicana se desarrolló como una industria de alta producción, y desde entonces se volvió imprescindible proteger a cada parvada contra la EN (4).
Además de las buenas prácticas de bioseguridad, el control de la EN consiste en la vacunación preventiva, utilizando la combinación de vacunas vivas e inactivadas (6); los tipos de vacuna y programas de vacunación varían dependiendo de la amenaza potencial, esto es, de la virulencia de la cepa presente, fin zootécnico de las aves y calendario de producción.
Aunque la vacunación contra la EN es una práctica normal de manejo, las cepas velogénicas son endémicas y responsables de importantes pérdidas directas e indirectas (8). Con las estrategias actuales de vacunas y vacunación, la mortalidad y morbilidad se han reducido pero no han eliminado la infección ni la excreción viral, lo cual es crítico para el control de la EN (5). Estos brotes en parvadas vacunadas sugieren que el nivel de cobertura de la vacunación es bajo, o que la vacunación no provee inmunidad perfecta permitiendo al virus diseminarse entre poblaciones. También es importante notar que en regiones donde no circula o aparentemente no circula el virus virulento, las empresas prefieren usar programas de vacunación que epidemiológicamente son no-óptimos debido a los efectos colaterales negativos de la vacunación (7), aunado al hecho de que la infección, diseminación y transmisión de la EN velogénica se puede presentar sin signos clínicos aparentes (3,7). Finalmente, no se puede ignorar que la presencia de altos niveles de anticuerpos maternos interfiere con el desarrollo de una inmunidad sólida después de la vacunación (1,9) al día de edad. Por lo tanto, los brotes continuos en parvadas comerciales vacunadas contra la EN demuestran que las estrategias actuales no son totalmente eficaces, éstas pueden ser mejoradas por una nueva generación de vacunas como son las vacunas vectorizadas.
La vacuna vectorizada de la Enfermedad de Marek HVT que expresa al gen de la proteína F del vEN (rHVT-NDV) han mostrado eficacia al aplicarse dentro de un programa de vacunación contra la EN (2). La protección que estas vacunas ofrecen se basa en la fuerte respuesta de tipo celular que el HVT induce y que adicionalmente, al expresar la proteína F del vEN, genera anticuerpos neutralizantes. Tan solo los anticuerpos contra la proteína F evitan la transmisión de célula a célula. La eficacia de la vacuna rHVTNDV ha sido probada en desafíos con cepas velogénicas en laboratorio (5), y también en condiciones de producción comercial en diferentes partes del mundo (Y. Gardin, comunicación personal) con considerable éxito.
El objetivo de éste trabajo es demostrar el nivel de protección generada por la vacuna rHVT_NDV incluida en programas de vacunación de pollos de engorda criados en condiciones comerciales y desafiadas en laboratorio con una cepa velogénica de la EN (Chimalhuacan) en términos de viabilidad y excreción viral, con la finalidad de mostrar que es factible su utilización en condiciones de producción propias de México.
Material y método
Para el desarrollo de este trabajo se corrieron cuatro experimentos con el mismo diseño, comparando parvadas vacunadas con rHVTNDV y virus vivos con parvadas con programas de vacunación que incluyen virus vivos e inactivos.
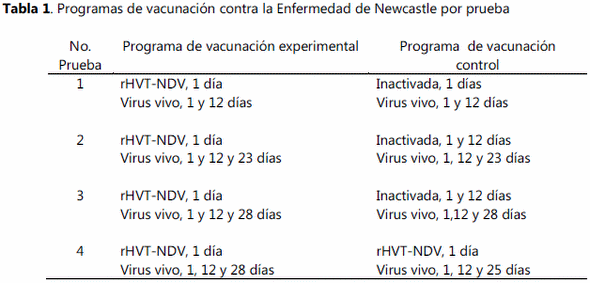
Aves. Se tomaron 80 pollos de engorda de 30 días de edad provenientes de 8 granjas distintas, ubicadas en cuatro zonas geográficas diferentes. De cada zona se tomaron 10 pollos de una granja vacunados contra la EN con rHVT-NDV más virus vivos y 10 pollos de otra granja diferente que fueron vacunados con virus vivos e inactivados (Tabla 1). Cada grupo de 10 aves se alojó en unidades de aislamiento con aire filtrado tipo Horsfall-Bauer junto con 5 aves SPF de la misma edad.
Vacunas. La vacuna rHVT-NDV (Vectormune® HVT_NDV) fue producida por Ceva-Biomune (USA). En todas las pruebas, la vacuna que se aplicó al día de edad fue la cepa PHY-LMV 42. La revacunación con virus vivos se realizó con: Prueba 1: PHY-LMV 42; Prueba 2: LaSota rND-AI; Prueba 3: LaSota y; Prueba 4: LaSota. Las vacunas inactivadas que se aplicaron en las pruebas 1,2 y 3 son elaboradas con la cepa LaSota, provenientes de diferentes laboratorios comerciales.
Desafío. A cada ave, incluyendo las aves SPF, se les aplicó 0.3 ml vía ocular de la cepa velogénica de la EN cepa Chimalhuacán con un título de 106 DIEP50. El virus de desafío fue originalmente aislado en México, y pertenece a la clase II, genotipo V, con un IPIC de 1.89.
Parámetros: Las aves fueron observadas por 14 días posdesafío (PD) por signos clínicos y mortalidad. El día que en que las aves fueron inoculadas se tomaron muestras de sangre para correr las pruebas de ELISA (IDEXX) y de HI (diluciones decimales seriadas) con 4 UH. A los siete días PD, se tomaron muestras de hisopos cloaca les para medir la excreción viral por medio de la prueba de Reacción en cadena por la Polimerasa de Tiempo Real (PCR-TR). La técnica de PCR-TR es la que se realiza en el laboratorio de diagnóstico de Investigación Aplicada, S. A. de C.V., Tehuacan Puebla). De cada grupo se tomaron 10 hisopos, mismos que se dividieron en dos pool.
Resultados
Viabilidad.. Ninguno de los cuatro grupos experimentales ni de los grupos control tuvo mortalidad, e incluso tampoco se presentaron signos clínicos que reportar. Con respecto a las aves SPF, todas murieron entre 3 y 6 días PD.
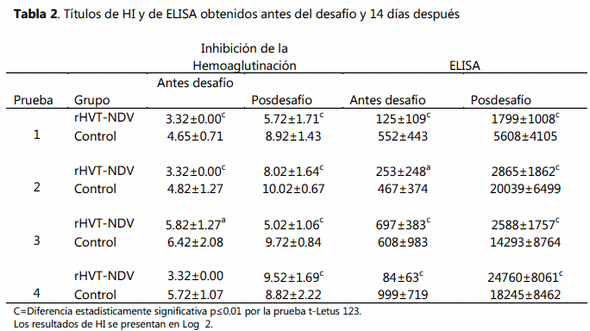
Serología. En la tabla 2 se presentan los resultados de las pruebas de HI y de ELISA Los títulos de HI obtenidos por los grupos vacunados con rHVT-NDV fueron bajos como se esperaba, dado que es la proteína F del vEN el que genera la respuesta inmune protectiva y no la Hemaglutinina, aunque tampoco ésta prueba fue capaz de detectar los anticuerpos generados por los virus vivos administrados en el mismo programa de vacunación. En los grupos vacunados con rHVT-NDV, el título HI inicial es el mínimo, excepto en la prueba 3 que probablemente se debió a que la aplicación de un virus vivo es la más reciente en comparación con otras pruebas. En todas las pruebas, el grupo control tuvo títulos de HI inicial más alto, y después del desafío mostraron una respuesta más alta con excepción de la prueba cuatro, debido a que en ésta ambos grupos recibieron la vacuna rHVT-NDV.
En este trabajo que se presenta, la prueba de ELISA-IDEXX no fue sensible para detectar los anticuerpos generados por la proteína F, y tampoco fue muy sensible al estímulo generado por los virus vivos aplicados en los mismos programas de vacunación.
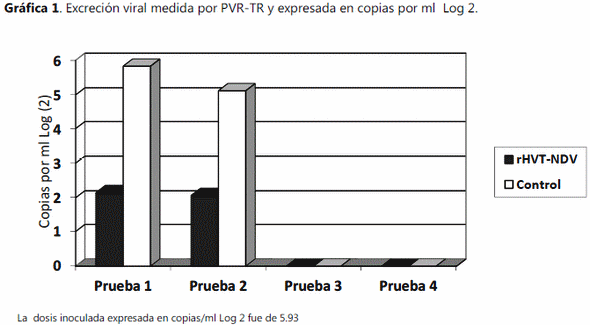
Excreción viral. Los resultados de prueba de excreción viral medida por PCR-TR se muestran en la gráfica 1. Las barras de la gráfica se agrupan en pool 1 y pool 2 de cada grupo.
Como se puede observar en la gráfica 1, solo se detectó excreción viral en las pruebas 1 y 2, muy probablemente relacionado con el programa de vacunación utilizado. La reducción en la excreción viral en estas pruebas fue significativamente menor en los grupos que recibieron la vacuna rHVT-NDV. En las mismas pruebas, las aves que recibieron vacuna inactivada, prácticamente no redujo la excreción viral, o la reducción de de menos de un logaritmo.
Discusión.
La vacuna rHVT-NDV es una vacuna vectorizada que utiliza al virus Herpes de Pavo HVT para expresar al gen de la proteína F del virus de la EN que se aplica en la incubadora al día de edad, o que pude aplicarse también in ovo para generar inmunidad contra las enfermedades de EN y de Marek. Después de correr cuatro pruebas de desafío en unidades de aislamiento con un virus velogénico de la EN cepa Chimalhuacan en pollos de engorda criados en granja, se pudo observar que:
Hubo 100% de protección contra signos clínicos y mortalidad en todos los grupos probados, tanto los experimentales vacunados con rHVT-NDV como en los grupos control. Si bien es cierto que no hubo diferencias en este punto de análisis, es importante para el objetivo del estudio hacer notar que la coincidencia en el resultado demuestra que todas las vacunas actuaron en tiempo y forma de acuerdo a su diseño, generando inmunidad suficiente. La norma mexicana para este tipo de desafíos indica que por lo menos el 80% de las aves desafiadas deben estar protegidas, y que por lo menos el 80% de las aves testigo deben morir o mostrar signos de la EN; en este caso la protección de los grupos probados fue de 100%, y así mismo, la mortalidad de todos los grupos de aves SPF murieron mostrando signos y lesiones de la EN, por lo que las cuatro pruebas se consideran satisfactorias.
El grupo de aves que recibieron la vacuna rHVT-NDV más virus vivos no generaron una respuesta serológica detectable por la prueba de HI y tampoco por la prueba de ELISAIDEXX. Es conocido que la respuesta inmune la genera la proteína F y no la proteína HN, así que se esperaba este resultado. Aunque también es importante mencionar que las dos pruebas serológicas tampoco fueron sensibles para detectar la respuesta generada contra las vacunas con virus vivos a los 35 días de edad. Así mismo, debido a la ausencia de respuesta serológica a la prueba de ELISA_IDEXX, se asume que es necesario contar con una prueba que detecte anticuerpos contra la proteína F del vEN. Como la respuesta serológica generada por el programa que recibió rHVT-NDV no es detectable por la prueba de HI, ésta prueba puede utilizarse como sistema DIVA (Differenciate Infected from Vaccinated Animals) para detectar infecciones por virus de campo.
En estos estudios, la respuesta serológica no estuvo relacionada con la protección como se ha mostrado en otros estudios donde se utilizan vacunas vivas e inactivadas. Este punto será importante para la interpretación de resultados serológicos cuando se utilice la vacuna rHVT-NDV en explotaciones comerciales.
En las pruebas de excreción viral con la prueba de PCR-TR, solo se detectaron virus en las pruebas 1 y 2, y aunque no tenemos una explicación o pruebas contundentes, especulamos que el tipo de vacunas con virus vivo que se usaron en estos programas incidieron en el resultado pues en las pruebas 3 y 4 se utilizaron vacunas conteniendo la cepa LaSota mientras que en las pruebas 1 y 2 se utilizaron vacunas apatógenas y LaSota recombinante, sin embargo, es necesario hacer pruebas complementarias para poder afirmarlo. Una observación importante es, que las aves vacunadas con rHVT-NDV en las pruebas 1 y 2 excretaron una cantidad significativa menor que las que recibieron vacunas inactivadas. La excreción viral de los grupos rHVT-NDV en las pruebas 1 y 2 redujeron en un 60-65% y totalmente en las pruebas 3 y 4, por lo que podemos afirmar que ésta vacuna tiene un fuerte potencial para reducir significativamente la transmisión del vEN velogénico de una manera más eficiente que los programas con vacunas inactivadas, ofreciendo un método de control de la EN más eficaz que lo que se utiliza actualmente.
Finalmente, el objetivo de este trabajo es conocer el potencial de la vacuna rHVT-NDV para ser utilizada dentro de un programa de vacunación contra la EN, en condiciones de producción comercial de pollo de engorda en un medio ambiente propio de las principales zonas avícola de México, de tal manera que concluimos que ésta vacuna puede ser incluida en programas de vacunación esperando un mejor desempeño que los programas convencionales.
Referencias.
1. Guittet B., Picault J., Bouquet J., Devaux B., Gaudry D. and Moreau Y. Vaccination of one day old chicks against Newcastle Disease using inactivated oil adjuvant vaccine and/or live vaccine. Avian Pathol. 7:15-27. 1978
2. Heckert R., Riva S., Cook J., McMillen J. Schwartz J. Onset of protective immunity in chickens after vaccination with a recombinant Herpesvirus of Turkeys vaccine expressing Newcastle Disease virus Fusion and Hemaglutinin- Neuroaminidase antigens. Avian Dis. 40 (4):770-7. 1996
3. Kapczynski D., King D., Protection of chickens against overt clinical disease and determination of viral shedding following vaccination with commercially available Newcastle Disease virus vaccines upon challenge with highly virulent virus
from the California 2002 exotic Newcastle Disease outbreak. Vaccine 23:3424-33. 2005
4. Moreno R. La Enfermedad de Newcastle y algunos avances recientes de diagnóstico. Ciencia Veterinaria (FMVZ-UNAM) 6:49-72. 1994
5. Rauw F., Gardin Y., Palya V., Anabari S., Lemarie S., Boschmans M. Improved vaccination against Newcastle Disease by in ovo recombinant HVT-NDV combined with an adjuvanted live vaccine at day old. Vaccine 28:823-833.2010
6. Senne D., King D., Kapczynski D., Control of Newcastle by vaccination. Dev. Biol. 119:165-70. 2004
7. VAnBoven M., Bouma A. Fabri T., Katsma E., Hartug L. and Koch G. Herd immunity to Newcastle Disease virus in poultry by vaccination. Avian Pathol. 37(1):1-5. 2008
8. Villegas P. Viral Diseases of respiratory syatem. Poultry Sci. 77:1143-45. 1998
9. Westbury H. Comparison of the immunogenicity of Newcastle Disease virus strains V4, Hitchner B1 and LaSota in chickens. Australian Veterinary J. 61:10-3. 1984
10. World Organization for Animal Health (OIE). International Animal Health Code, Paris In: OIE. 2003








.jpg&w=3840&q=75)